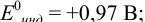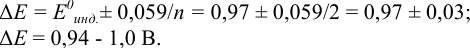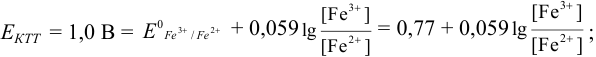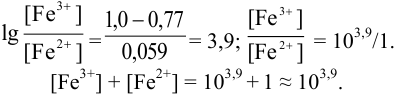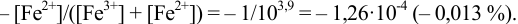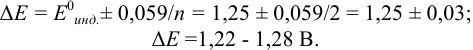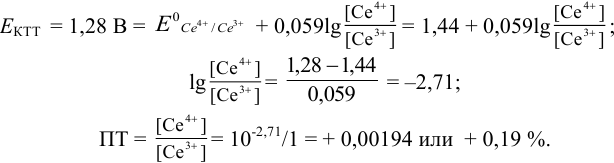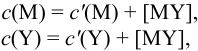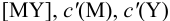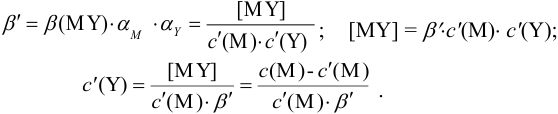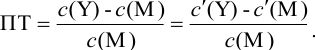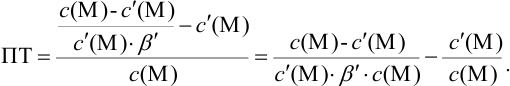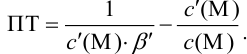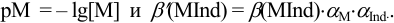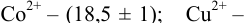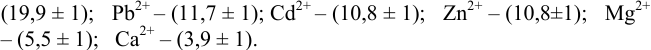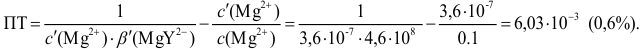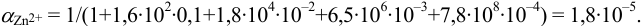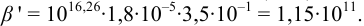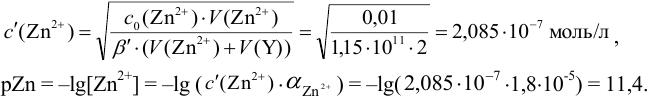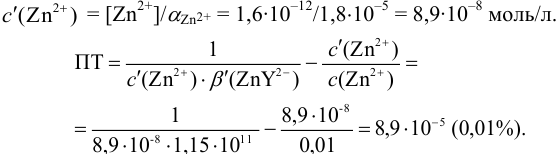Точность
зависит от многих факторов. Один из них
– точность отсчёта объёма рабочего
раствора по бюретке; обычно применяемой
для титрования. Погрешность отсчёта по
шкале, разделённой на десятые доли
миллилитра, составляет не менее 0,02 мл.
Оптимальный V
расходуемого рабочего раствора примем
равным 20мл.
Таким
образом, при принятых условиях
относительная погрешность ()отсчёта
объёма рабочего раствора по бюретке
составляет:
=
Погрешность
можно уменьшить, применяя специальные
приспособления, например весовую
бюретку, когда измеряют не V
раствора, а его массу. Однако такой
способ работы сопряжен со значительными
трудностями и увеличивает продолжительность
анализа. В обычных же условиях следует
считать неизбежной погрешность 0,1%.
Отсюда следует, что и при других операциях,
связанных с определением нет необходимости
стремиться обеспечить погрешность
меньшую, чем 0,1%.
Погрешности,
источниками которых являются неправильный
выбор индикатора, можно разделить на
две группы.
-
Индикатор
выбран так, что резкое изменение окраски
наблюдается после введения некоторого
избытка рабочего раствора по сравнению
с эквивалентным количеством. В этом
случае раствор перетитрован. -
Индикатор
выбран так, что переход окраски происходит
до того, как достигнута точка
эквивалентности. В этом случае раствор
недотитрован.
Погрешности
первой группы легко найти по объему
избытка рабочего раствора, прибавленного
для изменения окраски индикатора.
pH
в ТЭ HCOOH
равен 9,0 следовательно необходим
индикатор с рТ = 9, т.е. фенолфталеин.
Предположим, что индикатор выбран
неудачно – вместо фенолфталеина взят
тимолфталеин с рТ = 10. Индикатор изменит
цвет при рН=10 и раствор, следовательно,
будет перетитрован. Примем, что V
раствора в конце определения составляет
200мл. Для изменения цвета индикатора
необходимо прибавить такой избыток
раствора 0,2М раствора NaOH,
чтобы он был достаточен для создания
рН = 10. По соотношению между концентрацией
и объёмом находим V1M1
= V2M2,
где V1
– объём раствора в конце титрования
(200мл); M1
[H+]
= 10-10
или [OH—]
= 10-4,
M2
– молярность рабочего раствора NaOH
(0,2M),
V2
– необходимый
объём щелочи, необходимый для изменения
окраски индикатора,мл.
Таким
образом, для изменения цвета индикатора
необходимо прибавить избыток 0,2М раствора
NaOH
равный 0,1мл.
Если
принять, что исходное количество 0,2М
муравьиной кислоты составляет 100мл, то
относительная погрешность титрования
будет равна:
.
Погрешности
второй группы можно определить как
отношение неоттитрованного объёма
вещества к его первоначальному объёму,
или отношение концентрации неоттитрированной
части к первоначальной концентрации
вещества:
Во
многих случаях, когда погрешность не
слишком велика, принимают, что
первоначальная концентрация вещества
равна концентрации в оттитрированной
части:
,
Рассмотрим,
как влияет расхождение между рТ и рН
точки эквивалентности на погрешность
титрования 0,2M
раствора HCOOH
HCOOH
+ OH—
HCOO—
+ H2O
Равно
9,0.Предположим, что взят индикатор с рТ
= 9, в этом случае окраска изменится при
рН = 9, т.е. когда некоторая часть HCOOH
останется неоттитрированной, поэтому:
.
Отношение
в правой части уравнения находим из k
диссоциации кислоты:
.
Из
уравнения следует:,
где [H+]
– концентрация водородных ионов, при
которой индикатор изменяет окраску,
т.е. [H+]
= 10-9.
Принимая
во внимание, что ka
= 1,74 · 10-5,
получим
или
Δ=0,057 %
Таким
образом HCOOH
можно определить с погрешностью 0,057%,
если для титрования взят индикатор
фенолфталеин с рТ = 9.
При титровании
возможны случайные и систематические
погрешности (ПТ). Случайные погрешности
связаны с измерением объема и массы
навески, систематические- с несовпадением
ТЭ и конца титрования.
Случайные
погрешности обрабатывается
по законом математической статистики.
Они тем меньше, чем больше индекс крутизны
кривой титрования, поскольку стандартное
отклонение объема титранта St
связано с крутизной соотношением
где
s(V)
— стандартное
отклонение объема в конечной точке
титрования.
Индекс крутизны
при титровании слабых электролитов
меньше, чем при титровании сильных,
поэтому случайные погрешности в последнем
случае имеют меньшие значения.
Систематические
погрешности могут
быть положительными (перетитровывание)
и отрицательными (недотитровывание).
Для
оценки систематической погрешности
можно воспользоваться графическим и
расчетным способами. Графический
способ является
лишь ориентировочным. Опустим перпендикуляр
из точки с ординатой рТ на ось абсцисс.
Отрезок между полученным значением f
и f
в ТЭ и есть погрешность титрования.
При
расчетном
способе погрешность
вычисляют, используя формулы, связывающие
рН и f.
При недотитровывании ПТ=-(1-f),
при перетитровывании ПТ= f
-1. При титровании сильных кислот, для
которых
а с учетом изменения
объема
При титровании
сильных оснований
а с учетом изменения
объема
При
перетитровывании ПТ рассчитывают по
аналогичным формулам, но изменяет знак.
При
титровании слабых кислот относительная
погрешность титрования ПТ=f
-1. Учитывая, что
получаем
При титровании
слабого основания
Таблица №2.
Расчет индикаторных погрешностей кислотно-основного титрования
Согласно ионно-хромофорной теории индикаторов, интервал перехода окраски индикатора 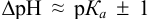
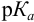
Таблица 8.12
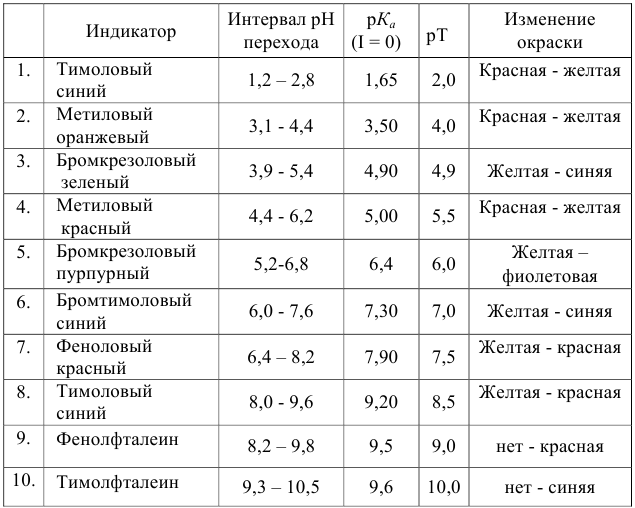
Важнейшие кислотно-основные индикаторы
При правильно выбранном индикаторе индикаторная ПТ не должна превышать заданную погрешность измерения объема раствора в титриметрии. Типы (виды) индикаторных ПТ кислотно-осиовиого титрования и названия, встречающиеся в разных учебниках и сборниках задач, происхождение погрешностей и формулы для расчета приведены в табл. 8.13. Формулы легко выводятся из определения погрешности титрования как отношения недотитро-ванного или перетитрованного количества кислоты или основания к первоначально взятому для титрования (то есть к произведению 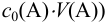
Таблица 8.13
Индикаторные погрешности кислотно-основного титрования
Пример 8.28.
Выберите подходящие индикаторы, определите тип индикаторных погрешностей и рассчитайте ПТ при титровании а) 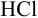
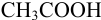
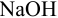
Решение:
а). Как следует из табл. 8.4 и рис. 8.1(1), для случая титрования 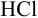

Однако используемые для расчета ПТ формулы показывают, что чем ближе рТ и 

Рассчитаем величину ПТ с двумя индикаторами: с рТ < 

С индикатором метиловым красным (рТ 5,5 < 
С индикатором фенолфталеином (рТ 9,0 > 
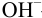
В данном случае оба индикатора пригодны, поскольку вычисленные значения ПТ не превышают заданную погрешность титрования (0,4%), но с метиловым красным систематическая индикаторная погрешность меньше.
б). При титровании 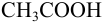



Например, при выборе фенолфталеина (рТ = 9,0):
а при выборе тимолфталеина (рТ = 10,0) погрешность возрастает в 10 раз:
Выбор фенолфталеина приводит к меньшей индикаторной погрешности титрования 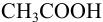
При титровании с индикаторами, для которых рТ < рНтэ, в растворе остается неоттитрованная слабая кислота, т. е. присутствует НА-ошибка (кислотная) со знаком «-» (см. табл. 8.13). Если использовать индикатор бромтимоловый синий (рТ 7,0), то вычисленная ПТ не удовлетворяет заданной точности, индикатор не пригоден:
или при проведении расчета по приближенной формуле:
Пример 8.29.
Какой индикатор позволяет оттитровать 0,1000 М гидразин 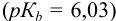
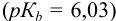
Решение:
Реакция титрования:
приводит к образованию слабой сопряженной кислоты 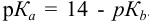
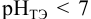
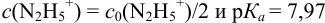
Сравнивая рТ индикаторов и 
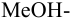
и с метиловым красным (рТ 5,5):
Из предложенных индикаторов метиловый красный позволяет провести титрование гидразина с меньшей погрешностью.
Расчет индикаторных погрешностей окислительно-восстановительного титрования
При использовании окислительно-восстановительных (редокс) индикаторов потенциал в ТЭ 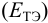

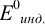
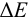
Таблица 8.14
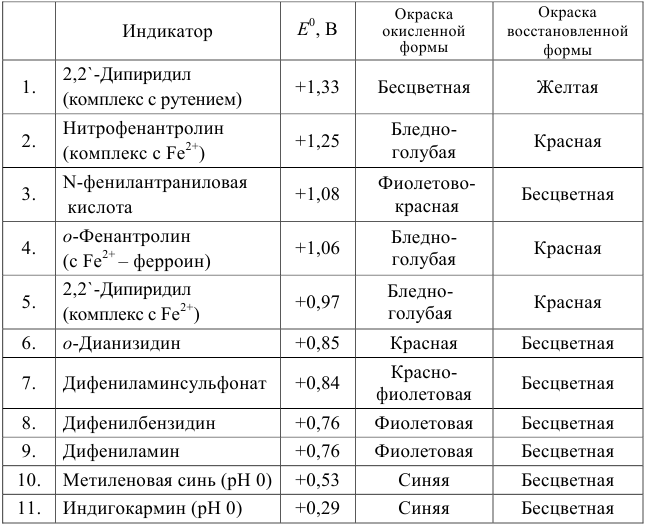
Примеры распространенных окислительно-восстановительных индикаторов
Полуреакция восстановления и интервал перехода индикатора:
Наиболее часто в полуреакции восстановления (окисления) индикатора участвуют 2 электрона. Для индикаторов №1 — №6 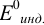
- сравнить
для выбора редокс-пары участников реакции титрования и уравнения Нернста для расчета ПТ.
Например, если 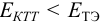
Сумма числителя и знаменателя здесь составляет 100 % титруемого вещества. Индикатор считается пригодным, если ПТ не превышает 0,1 -0,2%.
Пример 8.30.
Выберите подходящие индикаторы, определите тип индикаторных погрешностей и рассчитайте ПТ при титровании раствора соли 
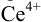
Решение:
Как следует из табл. 8.8 и рис. 8.3 (кривая 1, пример 8.25), область скачка (при относительной погрешности измерения объема 0,1 %) на кривой титрования 0,95 — 1,26 В, а 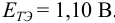
Выберем для рассмотрения порядка расчета два индикатора:
а) с 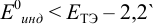
б) с 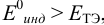
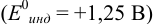
В случае а) интервал перехода индикатора:
Изменение окраски заканчивается при 
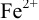
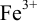
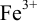

Тогда: ПТ =
В случае б) интервал перехода индикатора нитрофенантролина в виде комплекса с 
Изменение окраски заканчивается при 
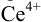
Тогда количество 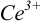
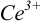
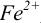
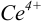
Таким образом, оба выбранных индикатора оказались приемлемыми.
Расчет индикаторных погрешностей комплексонометрического титрования
В конечной точке титрования общие концентрации определяемого иона с(М) и титранта c(Y) можно представить выражениями {для упрощения записи в общем виде упустим заряды ионов):
где 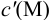
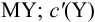
Условные константы устойчивости (см. выражение 8.16) связывают
Отсюда относительная погрешность титрования (ПТ) определяется выражением (с учетом (8.18) и (8.19)):
Подставляем в это уравнение выражение для 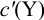
Вблизи ТЭ 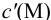
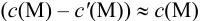
следовательно:
Выражение (8.21) тождественно выражению: 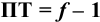
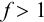
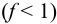
Конечная точка титрования определяется интервалом перехода окраски индикатора (интервалом рМ, в котором индикатор меняет свою окраску):
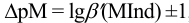
Интервал перехода окраски 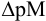
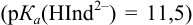
Пример 8.31.
Рассчитайте погрешность титрования 0,1 ОМ раствора 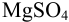

Решение:
В данных условиях 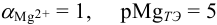
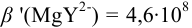
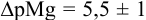
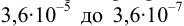
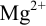
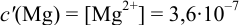
Погрешность титрования 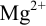
Пример 8.32.
Докажите возможность использования индикатора эриохром черный Т для титрования 0,010 М раствора 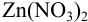

Решение:
1. Рассчитаем условную константу 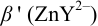
Общие константы устойчивости для аммиачных комплексов 
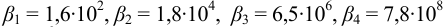

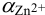
По табл. 7 и табл. 4 приложения находим 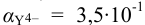
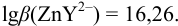

В точке эквивалентности:
Интервал перехода окраски индикатора эриохром черный Т в случае титрования ионов цинка при pH 10: 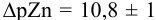
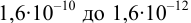

2. Конечная точка титрования наступает при [
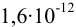

Эти примеры взяты со страницы примеров решения задач по аналитической химии:
Решение задач по аналитической химии
Возможны вам будут полезны эти страницы:
Аналогичная зависимость имеет место и при других видах реакций. Так, например, 0,1 и. раствор уксусной кислоты (Кк 1сл. = 2-10 . можно точно оттитровать 0,1 н. раствором едкой щелочи. Однако борную кислоту (Ккисл. = б-10 ) в тех же условиях уже нельзя титровать с удовлетворительной точностью. Наоборот, метаборнокислый натрий можно титровать соляной кислотой, а уксуснокислый натрий — нельзя. Некоторые из этих нри.меров расс.матриваются подробнее при изучении отдельных методов. Для вычисления ошибки титрования, обусловленной малым скачком (или, точнее, нерезким перегибом кривой титрования), вблизи точки эквивалентности имеется несколько методов, более или меиее сложных. Один из наиболее простых методов, предложенный К. Б. Яцимирским, кратко рассматривается ниже. [c.278]
В вычислении результатов титриметрических определений наименее точная цифра — число миллилитров титрующего раствора, израсходованного на титрование. Поскольку сотые доли миллилитра отмечаются лишь приблизительно, можно принять, что максимальная ошибка отмеривания не менее 0,02 мл. Ошибка от натекания также равна 0,02 мл. Таким образом, общая ошибка может доходить до 0,04 мл . При общем расходе титрующего раствора 20 мл это составит 0,2% отн. Отсюда следует, что, беря для анализа 1 г, вполне можно проводить отвешивание с точностью до 1 мг это дает относительную ошибку в 0,5 мг, или 0,05%. Если на титрование расходуется меньше 20 мл [c.11]
Этим уравнением можно пользоваться для вычисления относительной ошибки титрования и для определения допустимой степени разбавления раствора [261 ]. Предположим, что светопропускание измеряется с точностью 0,2%, т. е. что АТ = 0,002 и светопропускание в точке эквивалентности равно приблизительно 0,85. Уравнение (7,18) дает соответственно величину АС [c.189]
Весьма важное значение имеет правильное вычисление результатов объемного анализа. Все вычисления в объемном анализе рекомендуется производить со всей тщательностью и внимательностью, так как правильные результаты титрования, вследствие неправильно проведенных расчетов, дают неверный результат анализа. Всякое объемное определение включает две ошибки ошибку в концентрации титрующего раствора и ошибки титрования определяемого вещества. Эти ошибки могут компенсироваться в том случае, если концентрация титрующего раствора была установлена в тех же условиях, что и титрование анализируемого образца. Влияние случайных ошибок можно устранить, повторяя титрование несколько раз. Отклонение от среднего результата не должно превышать 0,3% относительных. Поэтому отсчеты объемов по бюретке необходимо вести с точностью до 0,02—0,03 мл. Например, три последовательных титрования дают следующие отсчеты 25,06 25,03 25,03 мл. Средний результат титрования должен быть записан в виде 25,04 мл. Если отклонения превышают допустимую величину, то такие результаты титрования не должны приниматься во внимание при вычислении среднего результата. Для повышения точности измерения объема применяют бюретки малого диаметра или весовые бюретки. [c.445]
Определение борной кислоты. Эту очень слабую кислоту можно непосредственно титровать щелочью, применяя тропеолин О или нитрамин в качестве индикаторов, в том случае, когда концентрация борной кислоты равна примерно 1 н. Рас-твором- свидетелем тогда может служить 0,05 М раствор карбоната натрия точность титрования 1—2%. При вычислении показателя титрования рТ следует иметь в виду, что борная кис-, лота ведет себя несколько ненормально ее константа диссоциации значительно возрастает с увеличением концентрации вследствие образования более сильной полиборной кислоты. Так, величина Ка при 18° оказалась равной 4,6-Ю в 0,1 М растворе, 2,6-10 в 0,25 М растворе и 1,19 10 в 0,5 Л1 растворе. Негели применил свои индикаторы помутнения для титрования борной кислоты. Он прибавлял в избытке щелочь, а затем оттитровывал обратно избыток последней 0,1 н. кислотой по индикатору изонитрозоацетил-/г-аминоазобензолу (стр. 63) до появления мути ошибки в его опытах доходили до 2—3%. [c.142]
Вычисление количества определяемого вещества основано на законе Фарадея. Чувствительность метода определяется чувствительностью способа индикации конца титрования и может быть доведена до микрограммовых количеств. Таким образом, метод пригоден для определения растворов как моляр-цай, так ц микромолярной концентрации. Точность метода определяется точностыо замера времени и силы тока. Ошибка определения составляет 0,1 %. Сксч)ость определения ка к правило, [c.257]
Анализируемый раствор подкисляют до pH 2—3 и на кончике шпателя добавляют твердую аскорбиновую кислоту (до полного исчезновения окраски железа) При тщательном перемешивании добавляют разбавленный раствор аммиака или буферный раствор до появления неисчезающей мути. На кончике шпателя вводят избыток КСК, разбавляют водой до 200—250 мл, добавляют 20 мл аммиачного буферного раствора с pH 10 и нагревают. Раствор светлеет и по достижении температуры 70—80 С становится светло-желтым. В теплый раствор добавляют из бюретки 0,1 М раствор комплексона III при тщателыюм перемешивании, пока раствор не станет прозрачным. Добавляют эриохром черный Т (смесь с НаС1 в соотношении 1 200) до сильной сине-зеленой окраски, и избыток комплексона III титруют 0,1 М раствором МдС12 до красной окраски и в заключение титруют раствором комплексона III до сине-зеленой окраски. Так много раз можно получить эквивалентную точку и при вычислении использовать среднее значение всех эквивалентных точек. Такой прием позволяет свести к минимуму капельную ошибку титрования и повысить точность определения. [c.79]
Хорошо известно, что количества кадия и натрия в смеси пх хлоридов могут быть вьлислены, если содержание хлорида точно известно (нанример, из результатов нотенциометрического титрования). Подобно этому, из результатов ионообменного определения сульфата можно вычислить состав смеси, состоящей из сульфатов калия и натрия. Оба определения дают достаточную точность только в том случае, если катионы присутствуют в смеси в приблизительно одинаковых количествах. Отсюда следует, что ценность этих определений для большинства практических целей весьма ограничена. Ионообменный метод, предложенный Габриэльсоном [35 J, дает значительно лучшие результаты, особенно в тех случаях, когда относительные количества солей различны (нанример, 10 и 90%). Изз чались только смеси хлоридов натрия и калия, и принцип метода легко может быть пояснен на этом примере. Пробу раствора выпаривают и остаток точно взвешивают. Другую пробу такого же объема пропускают через катионит, насыщенный одним из ионов раствора. Колонку промывают дистиллированной водой, вытекающий раствор и промывные воды выпаривают и остаток точно взвешивают. Из результатов этих взвешиваний состав раствора можно определить простым вычислением, причем максимальная относительная ошибка не превышает 2%. Метод можно использовать и для оиределения анионов в этом случае вместо катионита применяют анионит. [c.240]
Анализ составов равновесных фаз осуществляли рефрактометрически на приборе ИРФ-22 [5] и методом объемного титрования [6]. Точность измерения показателя преломления составила 0,0005. Среднеквадратичная ошибка при определении содержания уксусной кислоты в исследованных системах методом объемного титрования, вычисленная но формуле [7] [c.25]
Ошибка титрования вследствие разложения образующегося альдегидбисульфитного соединения. Для аналитических целей большое значение имеет вычисление по константе разложения альдегид-бисульфитного или кетон-бисульфитного соединения той части альдегида (или кетона), которая остается в свободном состоянии в растворе наряду с избытком бисульфита. Зная эту величину, можно вычислить точность аналитического определе- [c.245]
Эти данные можно использовать как для внесения соответствующих поправок, так и для вычисления минимального количества титруемого вещества при заданной точности определения. Если, например, на некоторое титрование теоретически необходимо затратить а миллиграмм-эквивалентов КМПО4, то в действительности затрачивается а -т миллиграмм-эквивалентов. Отсюда индикаторная ошибка О в процентах равна [c.149]
Расчет кривых титрования вблизи точки эквивалентности часто не отличается высокой точностью, поскольку он основан на использовании разности двух больших чисел, близких по абсолютному значению. Например, при вычислении концентрации AgNOз после добавления 25,10 мл 0,0100 М раствора AgNOз числитель в расчетной формуле (0,2510—0,2500) содержит лишь две значащих цифры следовательно, и AgNOз в лучшем случае можно вычислить с точностью до двух значащих цифр. Тем пе менее, чтобы уменьшить ошибку при округлении, мы провели этот расчет с точностью до трех цифр, а округлили после вычисления pAg. [c.195]


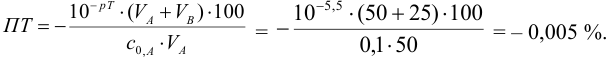
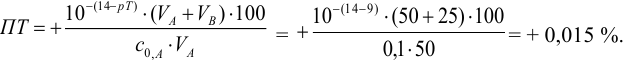
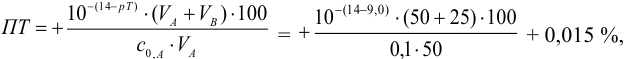
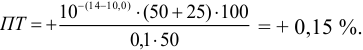
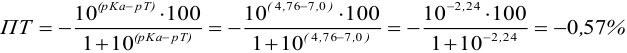
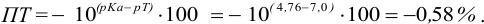
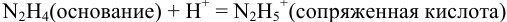
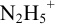
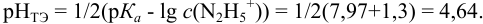
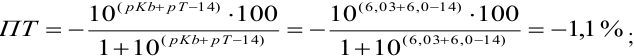
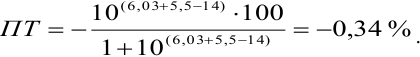

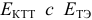 для выбора редокс-пары участников реакции титрования и уравнения Нернста для расчета ПТ.
для выбора редокс-пары участников реакции титрования и уравнения Нернста для расчета ПТ.