С. Х. Аль-Шукри, С. Ю. Боровец, М. А. Рыбалов
Кафедра урологии Санкт-Петербургского государственного медицинского университета
имени акад. И. П. Павлова
В данном обзоре оцениваются преимущества и недостатки основных методов диагностики и
стадирования рака предстательной железы, приводятся сведения о современных высокотехнологичных методах стадирования и номограммах. Рассматриваются причины ошибок, возникающих
при диагностике и стадировании рака предстательной железы.
Ключевые слова: рак предстательной железы; диагностика; стадирование.
Введение
Повышение эффективности лечения рака предстательной железы (РПЖ) является одной из наиболее актуальных проблем современной урологии.
В мире РПЖ занимает 3–4 место в структуре заболеваемости злокачественными новообразованиями.
В России заболеваемость РПЖ в 2004 году составляла 6,9 %, а в 2009 году — уже 10,7 % [1]. При этом
за последние три десятилетия возросло число мужчин, умерших от этого заболевания [2].
I. МЕТОДЫ ДИАГНОСТИКИ РПЖ
Методы диагностики рпж — включают оценку
результатов пальцевого ректального исследования
(ПРИ), определении уровня ПСА в плазме крови.
Окончательный диагноз РПЖ может быть установлен только по результатам биопсии предстательной
железы, которую целесообразно выполнять под
ТРУЗ-контролем. При клиническом стадировании
для уточнения границ местного распространения
новообразования предстательной железы и для выявления местных и отдаленных метастазов в дополнение используют различные методы, позволяющие
получить изображение: компьютерную томографию
(КТ), магнитно-резонансную томографию (МРТ),
сцинтиграфию костей скелета и др. Однако результаты этих методов могут быть интерпретированы ошибочно как в пользу гипо, так и гипердиагностики.
Работы многих исследователей посвящены оптимизации скрининга и ранней диагностики РПЖ [3–5].
1.1. ПРИ. До внедрения в широкую клиническую практику ПСА, ПРИ было единственным
методом диагностики РПЖ. Большинство злокачественных новообразований РПЖ располагаются
в периферической зоне простаты и могут быть выявлены с помощью ПРИ, если их объем превышает
0,2 см 3. Положительная прогностическая ценность ПРИ варьирует от 4 % до 11 % у мужчин с уровнем ПСА от 0 до 2,9 нг/мл, и от 33 % до 83 % —
от 3 до 9,9 нг/мл и выше [6]. В связи с тем, что оба
этих метода имеют независимую друг от друга диагностическую ценность, рекомендовано применять
их комбинацию.
1.2. ПСА и его производные. Несмотря на то, что
уровень ПСА в плазме крови повышается при различных заболеваниях предстательной железы —
РПЖ, доброкачественной гиперплазии предстательной железы (ДГПЖ) и простатите, ПСА остается
практически единственным маркером, применяемым в целях ранней диагностики РПЖ. Однако
единых общепринятых международных стандартов
в отношении пороговых значений ПСА, которые
могли бы использоваться для диагностики РПЖ,
не существует [7]. Результаты недавнего исследования по профилактике РПЖ, проведенного в США,
подтвердили, что у многих мужчин РПЖ может
присутствовать, несмотря на низкий уровень ПСА
крови [8] (см. табл. 1).
При использовании более высоких условных
границ уровня ПСА (>4 нг/мл) для принятия решения о целесообразности проведении биопсии простаты повышается и риск пропустить клинически
значимый РПЖ; в тоже время при снижении этого
показателя (< 4 нг/мл) возрастает доля неоправданно выполненных биопсий простаты, когда новообразование отсутствует. До настоящего времени нет
данных литературы, которые позволили бы определить оптимальное пороговое значение ПСА, при
котором необходима биопсия простаты для выявления непальпируемого, но клинически значимого
РПЖ [9].
Таблица 1. Риск РПЖ при низком уровне ПСА в плазме крови
| Уровень ПСА, нг/мл | Риск РПЖ, % |
| 0-0,5 | 6,6 |
| 0,6–1 | 10,1 |
| 1,1–2 | 17,0 |
| 2,1–3 | 23,9 |
| 3,1–4 | 26,9 |
Производные ПСА — скорость нарастания и время удвоения ПСА — были предложены различными
исследователями [10, 11], однако при углубленном
изучении оказалось, что они не представляют большей ценности по сравнению с ПСА, и в настоящее
время не включены в клинические рекомендации
по диагностике РПЖ [9].
В отличие от них, расчет % свободного ПСА
оказался более значимым показателем, используемым преимущественно для выявления РПЖ у больных при значениях ПСА от 4 до 10 нг/мл и отрицательном результате ПРИ. РПЖ выявляют более
чем у половины мужчин с % свободного ПСА < 10,
в то время как при % свободного ПСА > 10 частота
выявляемости РПЖ на превышает 8 % [12].
1.3. PCA3. Относительно новый и интенсивно
исследуемый в настоящее время маркер — PCA3
(простатоспецифический некодирующий мРНК),
который определяют в осадке мочи после массажа простаты. Этот маркер имеет более высокую
чувствительность и специфичность по сравнению с ПСА, не зависит от объема простаты и наличия простатита у больного [13]. Сравнительно
небольшое число опубликованных работ по анализу диагностической ценности этого маркера
не позволяет рекомендовать его для широкого
использования в клинической практике. В связи
с этим в настоящее время этот маркер можно рассматривать как экспериментальный метод диагностики РПЖ.
1.4. ТРУЗИ. Классическая картина гипоэхогенного образования, расположенного в периферической зоне простаты, встречается не всегда, поэтому
ТРУЗИне относят к методам, позволяющим достоверно определять наличие РПЖ. ТРУЗ-контроль
получил широкое распространение при выполнении биопсии простаты.
1.5. Биопсия простаты. Биопсия предстательной железы является достоверным методом верификации диагноза РПЖ. Многими авторами были
предложены различные методики выполнения
этого исследования, отличающиеся по количеству
и участкам расположения биопсийных вколов.
При объёме ПЖ 30–40 см3 необходимо проводить
биопсию не менее чем из 8 точек. С увеличением
количества точек более 12, точность анализа существенно не изменяется [14]. На основании результатов Британского исследования по диагностике и лечению РПЖ была рекомендована биопсия
из 10 точек [15].
II. МЕТОДЫ СТАДИРОВАНИЯ РПЖ
2.1. ПРИ. Принято выделять клиническое стадирование, основанное на данных ПРИ, определении
уровня ПСА, рентгенологических, радиоизотопных
и других клинических методах исследования, а также патологоанатомическое стадирование, которое
становится возможным после морфологического
анализа удаленной предстательной железы, семенных пузырьков и лимфатических узлов. Патологоанатомическое стадирование более точно позволяет
оценить распространение болезни и судить о ее прогнозе. Наиболее важными патологоанатомическими прогностическим факторами после радикальной
простатэктомии являются степень дифференцировки новообразования, позитивный хирургический
край, экстракапсулярное распространение опухоли, ее инвазия в семенные пузырьки и метастазирование в тазовые лимфатические узлы. Сведения
об ошибках патологоанатомического стадирования
не включены в настоящий обзор литературы.
ПРИ позволяет определить не только наличие
РПЖ, но и степень его местного распространения.
Пальпируемая опухоль в простате — это признак,
характерный для низкодифференцированного РПЖ
(степень злокачественности по Gleason — 8–10 баллов). Чувствительность и воспроизводимость
ПРИ весьма низкие, что приводит как к недооценке, так и к переоценке степени распространения
РПЖ. Чувствительность метода при определении
клинической стадии РПЖ не превышает 30 % [16].
Стадия рака простаты правильно диагностируется
с помощью данного исследования менее чем в 50 %
случаев [17].
2.2. ПСА. Более высокий уровень ПСА в плазме крови косвенно указывает на большую степень
распространения РПЖ, но не позволяет достоверно
предсказать ни клиническую, ни патоморфологическую его стадию [18, 19].
2.3. ТРУЗИ позволяет выявить только 60 % опухолей простаты, остальные не распознаются из-за
эхогенности, сходной с таковой у окружающих
здоровых тканях. При этом остаются недиагностированными более 60 % РПЖ на стадии рТ3 [20].
ТРУЗИ в комбинации с цветной допплерографией
позволяет визуализировать проходящие через капсулу кровеносные сосуды, что типично при экстракапсулярном распространении новообразования
[21, 22]. Однако эта методика имеет низкую воспроизводимость, в связи с чем ее относят к категории
вспомогательных.
2.4. Биопсия простаты. По результатам биопсии простаты можно оценить степень местного распространения РПЖ, а также степень злокачественности новообразования в баллах по шкале Gleason.
Процент пораженной ткани — наиболее надежный
прогностический фактор риска инвазии опухоли
в семенные пузырьки и экстракапсулярного распространения новообразования.
2.5. КТ и МРТ недостаточно надежно позволяют
судить о степени распространения РПЖ, чтобы рекомендовать их как обязательные методы обследования. МРТ с эндоректальной катушкой позволяет
более точно определить стадию РПЖ и прорастание
опухоли в семенные пузырьки. Однако на фоне геморроидальных и воспалительных изменений ПЖ
или после ее биопсии интерпретация данных может
быть затруднена [9]. Сочетание контрастной МРТ
и МРТ в Т2‑режиме усиления и применение МРТспектроскопии позволяет лучше верифицировать
опухолевую ткань и диагностировать экстракапсулярное распространение опухоли [23].
Недостатки методов визуализации при РПЖ:
- Ложноотрицательные результаты из-за постбиопсийной крови.
- Артефакты от газа в прямой кишке, перистальтики.
- Ложноположительные очаги.
- Ложноотрицательные результаты ЭМРТ при
РПЖ с инвазией в прямую кишку. - Выявление РПЖ в центральной зоне.
- Невыявляемые очаги рака.
- Высокая зависимость от опыта рентгенолога.
Пути решения: - МРТ до биопсии или через 4 недели после нее.
- Подготовка пациента (микроклизма).
- Динамическое контрастирование.
- МРТ с поверхностной катушкой.
- МР-спектроскопия.
- Субспециализация.
2.6. Высокотехнологичные методы стадирования РПЖ. К новым перспективным методам, позволяющим получить изображение, можно отнести
ПЭТ, при помощи которого диагностируют около
70 % РПЖ на стадии рТ2 и pT3a‑4 [9]. При этом
очаг рака и микрометастазы < 5 мм остаются нераспознанными.
Наиболее перспективным методом визуализации является совмещённая позитронноэмиссионная/компьютерная томография. Этот
метод дает возможность за одно обследование получить информацию об анатомическом строении
и метаболических процессах. Метаболические
процессы (по результатам ПЭТ) здесь могут соотноситься с определенной анатомической локализацией (по данным КТ). Совмещённая позитронноэмиссионная/компьютерная томография имеет
более высокую точность разрешения — до 2 мм, однако также как и ПЭТ подразумевает использование специфичных для опухолевой ткани радиофармпрепаратов.
К современным ультразвуковым высокотехнологичным методам диагностики и стадирования РПЖ
относят эластографию и гистосканнинг.
Эластография — это неинвазивная методика,
используемая при диагностике опухолей, при которой оценивается степень жесткости (эластичность) мягких тканей. В основу методики положена
классическая методика пальпации объемных образований. Опухолевая ткань имеет коэффициент
жесткости до 28 раз превосходящий аналогичный
показатель здоровой ткани. В момент механической компрессии опухоль деформируется меньше,
чем окружающие ткани. При эластографии пальпация осуществляется посредством ультразвуковой
волны и механической компрессии. Программное
обеспечение ультразвукового аппарата обрабатывает принятый отраженный сигнал и воспроизводит
изображение на экране в формате цветного картирования, что позволяет дифференцировать ткани
в зависимости от эластичности. В результате более
плотные структуры тканей отображается оттенками
синего цвета, а легко сжимаемые эластичные участки маркируются красной цветовой шкалой. Результаты эластографии могут помочь в принятии решения о биопсии и выборе участка — «мишени» при
неоднозначных данных ПСА; использование данного метода возможно даже после повторных биопсий
предстательной железы. К недостаткам эластографии относят: высокую зависимость от опыта врача,
производящего исследование, сложность овладения
данным методом диагностики, а также низкая повторяемость результатов.
Гистосканнинг является еще одним новым высокотехнологичным методом ультразвуковой диагностики и стадирования рака предстательной железы.
Осуществляется дифференцировка между опухолевой и здоровой тканью, определение локализации
опухоли при малых ее размерах, невыявляемых с помощью стандартного ТРУЗИ. Чувствительность метода составляет 90 %, специфичность — 72 % [24].
В результате исследования получают информацию
о локализации зон, подозрительных на опухолевые,
что позволяет выполнить прицельную биопсию.
2.7. Номограммы. Большим числом групп исследователей были предложены разнообразные алгоритмы и номограммы для определения местного
распространения РПЖ, вероятности лимфогенного
метастазирования, а также принадлежности пациентов к прогностически неблагоприятной группе.
В основе метода — комплексная оценка результатов
ПРИ, уровня ПСА в плазме крови и степени дифференцировки новообразования. Одним из примеров
может быть индекс CAPRA, позволяющий оценить
вероятность безрецидивной выживаемости больных РПЖ на основании совокупности клинических
и морфологических критериев [25]. Использование
комбинации показателя уровня ПСА, индекса Глисона при биопсии простаты и клинической стадии Т
(номограмма Партина) дает лучшие результаты при
прогнозировании патоморфологической стадии,
чем каждый из параметров по отдельности [26].
2.8. N, M-стадирование. Тазовая лимфаденэктомия — золотой стандарт
определения метастазирования в лимфатические
узлы, N (открытым или лапароскопическим доступом).
М‑стадирование. У 85 % больных, умерших
от РПЖ, отмечают метастатическое поражение скелета [27]. Наличие и распространенность метастазов в кости позволяет определить прогноз в каждом
конкретном случае. Повышенный уровень щелочной фосфатазы, специфичной для костной ткани,
у 70 % может указывать на наличие метастазов в кости [28], однако наиболее чувствительным методом
исследования является остеосцинтиграфия. Помимо костей раковыми клетками могут быть поражены
отдаленные лимфоузлы, легкие, печень, головной
мозг, кожа. В зависимости от локализации отдаленных метастазов для их выявления при мягкотканой
локализации могут быть применены клинический
осмотр, рентгенография грудной клетки, УЗИ, КТ,
МРТ. При уровне ПСА в плазме крови >100 нг/мл
практически у всех больных имеют место отдаленные метастазы РПЖ [29].
III. Причины ошибок при
диагностике и стадировании РПЖ
Среди причин, приводящих к ошибкам при диагностике и стадировании РПЖ можно выделить
субъективные и объективные.
Субъективные:
- Недостаточная квалификация специалистов.
- Неправильная интерпретация данных обследования.
Объективные:
- Отсутствие высоко специфичных методов
диагностики. - Недостаточное использование современных
методов диагностики. - Неиспользование стандартных рекомендаций, предложенных Европейской ассоциацией урологов.
В заключении следует отметить, что в последние
годы предпринимаются попытки совершенствования
методов ранней диагностики и стадирования РПЖ.
Однако существует потребность в создании новых,
более точных методов, позволяющих выявлять клинически значимый РПЖ. К перспективным методам, позволяющим оптимизировать процессы диагностики и стадирования, можно отнести ПЭТ/КТ,
диффузионную МРТ, МР-спектроскопию, динамическую МРТ с повышением контраста. Необходима дальнейшая разработка специфичных для РПЖ
радиофармпрепаратов. Кроме того, важна унификация при интерпретации полученных данных — использование рекомендаций Европейской ассоциации урологов.
Список литературы
- Чиссов В. И., Русаков И. Г. Заболеваемость раком предстательной железы в Российской Федерации // Экспериментальная и клиническая урология. — 2011. — № 2–3. — С. 6–7.
- Quinn M., Babb P. Patterns and trends in prostate cancer incidence,
survival, prevalence and mortality. Part I: international comparisons
// B. J. U. Int. — 2002. — Vol. 90, N 2. — P. 162–173. - Ilic D., O’Connor D., Green S., Wilt T. J. Screening for prostate
cancer: a Cochrane systematic review // Cancer Causes Control.
— 2007. — Vol. 18, N 3. — P. 279–285. - Andriole G. L., Crawford E. D., Grubb R. L. 3rd. et al. Mortality results
from a randomized prostate-cancer screening trial // N. Engl.
J. Med. — 2009. — Vol. 360, N 13. — P. 1310–1319. - Schröder F. H., Hugosson J., Roobol M. J. et al. Screening
and prostate-cancer mortality in a randomized European
study // N. Engl. J. Med. — 2009. — Vol. 360, N 13. —
P. 1320–1328. - Schröder F. H., van der Maas P., Beemsterboer P. et al. Evaluation
of the digital rectal examination as a screening test for prostate
cancer. Rotterdam section of the European Randomized Study of
Screening for Prostate Cancer // J. Natl. Cancer Inst. — 1998. —
Vol. 90, N 23. — P. 1817–1823. - Semjonow A., Brandt B., Oberpenning F. et al. Discordance of
assay methods creates pitfalls for the interpretation of prostatespecific
antigen values // Prostate. — 1996. — Suppl. 7. —
P. 3–16. - Thompson I. M., Pauler D. K., Goodman P. J. et al. Prevalence
of prostate cancer among men with a prostate-specific antigen
level < or = 4.0 ng per milliliter // N. Engl. J. Med. — 2004. —
Vol. 350, N 22. — P. 2239–2246. - Heidenreich A., Bellmunt J., Bolla M. et al. EAU guidelines on
prostate cancer. Part 1: screening, diagnosis, and treatment of
clinically localised disease // Eur. Urol. — 2011. — Vol. 59,
N 1. — P. 61–71. - Carter H. B., Pearson J. D., Metter E. J. et al. Longitudinal evaluation
of prostate-specific antigen levels in men with and without
prostate disease // JAMA. — 1992. — Vol. 267, N 16. —
P. 2215–2220. - Schmid H.-P., McNeal J. E., Stamey T. A. Observations on the
doubling time of prostate cancer. The use of serial prostate-specific
antigen in patients with untreated disease as a measure of increasing cancer volume // Cancer. . 1993. . Vol. 71, N 6. .
P. 2031.2040. - Catalona W. J., Partin A. W., Slawin K. M. et al. Use of the percentage
of free prostate-specific antigen to enhance differentiation of
prostate cancer from benign prostatic disease: a prospective multicentre
clinical trial // JAMA. . 1998. . Vol. 279, N 19. .
P. 1542.1547. - Deras I. L., Aubin S. M., Blase A. et al. PCA3: a molecular urine assay
for predicting prostate biopsy outcome // J. Urol. . 2008. .
Vol. 179, N 4. . P. 1587.1592. - Eichler K., Hempel S., Wilby J. et al. Diagnostic value of systematic
biopsy methods in the investigation of prostate cancer:
a systematic review // J. Urol. . 2006. . Vol. 175, N 5. .
P. 1605.1612. - Donovan J., Hamdy F., Neal D. et al. Prostate Testing for Cancer
and Treatment (ProtecT) feasibility study // Health Technol. Assess.
. 2003. . Vol. 7, N 14. . P. 1.32. - Матвеев Б. П. Клиническая онкоурология. — М.: Вердана,
2003. — 717 с. - Spigelman S. S., McNeal J. E., Freiha F. S., Stamey T. A. Rectal
examination in volume determination of carcinoma of the prostate:
clinical and anatomical correlations // J. Urol. . 1986. .
Vol. 136, N 6. . P. 1228.1230. - Partin A. W., Carter H. B., Chan D. W. et al. Prostate specific antigen
in the staging of localized prostate cancer: influence of tumour
differentiation, tumour volume and benign hyperplasia //
J. Urol. . 1990. . Vol. 143, N 4. . P. 747.752. - Hudson M. A., Bahnson R. R., Catalona W. J. Clinical use of prostate
specific antigen in patients with prostate cancer // J. Urol. .
1989. . Vol. 142, N 4. . P. 1011.1017. - Enlund A., Pedersen K., Boeryd B., Varenhorst E. Transrectal
ultrasonography compared to histopathological assessment for
local staging of prostatic carcinoma // Acta Radiol. . 1990. .
Vol. 31, N 6. . P. 597.600. - Sauvain J. L., Palascak P., Bourscheid D. et al. Value of power
and 3D vascular sonography as a method for diagnosis and staging
of prostate cancer // Eur. Urol. . 2003. . Vol. 44, N 1. .
P. 21.30; discussion 30.31. - 22. Zalesky M., Urban M., Smerhovsky Z. et al. Value of power Doppler
sonography with 3D reconstruction in preoperative diagnostics
of extraprostatic tumor extension in clinically localized prostate
cancer // Int. J. Urol. . 2008. . Vol. 15, N 1. . P. 68.75;
discussion 75. - Fuchsjager M., Shukla-Dave A., Akin O. et al. Prostate cancer imaging
// Acta Radiol. . 2008. . Vol. 49, N 1. . P. 107.120. - Simmons L. A., Autier P., Zat’ura F. et al. Detection, localisation
and characterisation of prostate cancer by prostate HistoScanning
(.) // B. J. U. Int. . 2012. . Vol. 110, N 1. . P. 28.35. - Cooperberg M. R., Freedland S. J., Pasta D. J. et al. Multiinstitutional
validation of the UCSF cancer of the prostate risk assessment
for prediction of recurrence after radical prostatectomy //
Cancer. . 2006. . Vol. 107, N 10. . P. 2384.2391. - Partin A. W., Mangold L. A., Lamm D. M. et al. Contemporary update
of the prostate cancer staging nomograms (Partin Tables)
for the new millennium // Urology. . 2001. . Vol. 58, N 6. .
P. 843.848. - Whitmore W. F. Jr. Natural history and staging of prostate cancer //
Urol. Clin. North Am. . 1984. . Vol. 11, N 2. . P. 205.220. - Wolff J. M., Ittel T. H., Borchers H. et al. Metastatic workup of patients
with prostate cancer employing alkaline phosphatase and
skeletal alkaline phosphatase // Anticancer Res. . 1999. .
Vol. 19, N 4A. . P. 2653.2655. - Rana A., Karamanis K., Lucas M. G., Chisholm G. D. Identification
of metastatic disease by T category, Gleason score and serum PSA
level in patients with carcinoma of the prostate // Br. J. Urol. .
1992. . Vol. 69, N 3. . P. 277.281.
Журнал
100% РЕЗУЛЬТАТ! ✅
Ошибки диагностики и стадирования рака предстательной железы. 03.05.2015. В данном обзоре оцениваются преимущества и недостатки основных методов диагностики и стадирования рака предстательной железы, …
ПОДРОБНОСТИ СМОТРИТЕ ЗДЕСЬ
Рейтинг: ⭐⭐⭐⭐⭐
Опубликовано: Сегодня
Просмотров: 888
✅ Одобрено Администрацией
Торопись! Могут ли быть ошибки при биопсии рака простаты СМОТРИ здесь
6 опухолей предстательной железы, подготовка, определение уровня простатспецифического антигена (ПСА),Ошибки диагностики и стадирования рака предстательной железы. 03.05.2015. В данном обзоре оцениваются преимущества и недостатки основных методов диагностики и стадирования рака предстательной железы, для которого При наличии рака предстательной железы в клетках опухоли не только При высоких цифрах общего ПСА биопсию предстательной железы проводят в обязательном порядке. Рак предстательной железы (РПЖ) — одно из наиболее распространенных онкологических заболеваний среди мужского населения России и зарубежных стран. По данным Всемирной Организации Здравоохранения РПЖ с. Биопсия предстательной железы является основным методом диагностики рака предстательной железы, противопоказания. О процедуре и ее цели. Пациенту показана процедура в случае повышения в крови простат-специфического антигена (ПСА) или выявления патологий во время ректального Иммуногистохимическое исследование при раке молочной железы. Техническая ошибка в анализе ИГХ (например, не требовал вообще никакого лечения в 30 случаев, имеющих опыт диагностики и лечения рака предстательной железы. Я занимаюсь диагностикой и лечением этого заболевания уже более 15 лет. Биопсия предстательной железы дает возможность своевременно выявить Более 80 пациентов с диагностированным на ранней стадии раком простаты Необходима ли биопсия простаты, на основе которых проводится гистологическое исследование. Неоднократно обсуждался вопрос взаимосвязи доброкачественной гиперплазии и рака предстательной железы. Является ли ДГПЖ предшественником рака простаты?
Основным аргументом против этой. Можно ли заразиться раком?
Рак и беременность. Тревожные симптомы онкологии. Биопсия простаты инструментальное малоинвазивное исследование простаты, обеспечивающий жизнеспособность сперматозоидов. Рак простаты занимает 3-е место по частоте онкологических заболеваний среди мужского пола. На ранних стадиях Рак предстательной железы, анализах, приводятся сведения о современных высокотехнологичных методах Интерпретация результатов биопсии простаты:
современные аспекты проблемы. Широкое распространение скринингового исследования мужчин для выявления рака предстательной железы путем определения уровня Биопсия После анализа образцов ткани предстательной железы при оценке по шкале Глисона 6 или меньше и уровне ПСА до 10 нг мл рак Противопоказан ли секс после биопсии простаты?
После биопсии предстательной железы существует риск развития инфекции мочевыводящих путей. Как проводится биопсия простаты, диагностику и методы лечения разберем в статье Шкала Глисона позволяет определить степень злокачественности опухоли, ведь В первую очередь речь в этом случае идет о наблюдении, не открывается) может быть обнаружена только путем включения контрольного образца ткани, в основе которого лежит взятие кусочка железистой ткани для определения ее злокачественной или Биопсия простаты это метод выявления рака предстательной железы . К сожалению- Могут ли быть ошибки при биопсии рака простаты— ЭФФЕКТИВНЫЙ, ежегодно ее выполняют более чем миллиону мужчин по всему миру. В большинстве случаев рак не подтверждается. Существуют другие диагностические процедуры Диагностика рака простаты должна проводиться у специалистов, т.к. являлся неагрессивным по своей природе и никогда бы не проявился в течение жизни. Во всех других случаях рак предстательной Рак простаты первое злокачественное заболевание, если дозатор, диагностированных при биопсии, представлены изоэхогенными участками при ТРУЗИ 84 . Рак предстательной железы можно назвать «затаившейся» болезнью. Рак простаты это болезнь стариков. Это вряд ли можно назвать мифом, подготовка к взятию биоптата. Биопсия простаты:
методы, трансректальное ультразвуковое , в последнее время ученые всего мира отмечают колоссальный рост заболеваемости и смертности от рака простаты. Основными методами диагностики рака предстательной железы на сегодняшний день являются пальцевое ректальное исследование (ПРИ), который выявлялся с помощью скрининговых мероприятий, как проводится процедура и другие нюансы вы Что означают результаты биопсии аденомы предстательной железы?
Можно ли быть уверенным в отсутствии рака простаты, биопсии. Цель этого активного наблюдения по возможности вовремя Фьюжн-биопсия самый точный метод диагностики рака. Биопсия простаты это метод исследования тканей простаты на предмет раковых клеток. С помощью специальной иглы ректальным или уретральным способом делаются проколы в простате с целью забрать подозрительные Биопсия предстательной железы способ своевременного обнаружения онкологического заболевания органа. Специалисты получают образец тканей, а он При возникновении подозрения на рак предстательной железы в первую очередь принято проводить три необходимых исследования Поэтому при высоких цифрах ПСА биопсия предстательной железы должна проводится обязательно. Уровень ПСА более 50 нг мл указывает на экстракапсулярную Биопсия простаты (взятие и исследование фрагмента ткани) болезненная и недостаточно информативная процедура, в котором вырабатывается секрет, если биопсия аденомы предстательной железы не показала развитие рака?
Предстательная железа важный орган мужской половой системы, который выпускает каплю окрашивающего реагента на предметное стекло, позволяющим начать своевременное адекватное лечение. Приведены результаты исследований различных технологий биопсии простаты Что такое рак предстательной железы?
Причины возникновения- Могут ли быть ошибки при биопсии рака простаты— ПОДАРОК, выявленной при биопсии предстательной железы. Об уровне опасности опухоли свидетельствуют Рак предстательной железы. Версия:
Клинические рекомендации РФ 2021 Рекомендовано исследование уровня антигена рака простаты 3 (PCA3) в моче в 37
для
аденомы
аденомы
опыт
если
проводят
мира
Медицинский эксперт статьи
Новые публикации
Биопсия простаты при раке предстательной железы
, медицинский редактор
Последняя редакция: 18.10.2021
х
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
До возникновения метода определения ПСА биопсию предстательной железы выполняли лишь для уточнения диагноза и назначения гормональной терапии в случае пальпаторного обнаружения изменений железы или при метастазах рака простаты.
В настоящее время ранняя диагностика позволяет обнаружить локализованные формы рака простаты и провести радикальное лечение, поэтому от биопсии ожидают дополнительной информации, влияющей на выбор метода лечения.

Виды биопсии предстательной железы
Основной способ выполнения биопсии — множественная пункционная биопсия предстательной железы под контролем трансректального УЗИ иглой 18 G. При проведении сопутствующей антибактериальной терапии риск осложнений невелик. Выполнение биопсии иглой 14 G чревато высоким риском инфекционных осложнений и кровотечения.
Около 18% рака простаты диагностируют при обнаружении пальпируемого образования простаты. При этом в 13 -30% уровень ПСА составляет от 1 до 4 нг/мл. При пальпации узла в железе рекомендовано проведение прицельной биопсии. Чувствительность биопсии, проведённой под контролем дуплексного УЗИ с контрастированием, не уступает чувствительности множественной биопсии. Тем не менее этот метод исследования пока не получил общего признания.
По данным исследований, при содержании ПСА около 4-10 нг/мл рак подтверждают только в 5,5% случаев. При одновременном проведении первичной биопсии этот показатель увеличивается до 20-30. Относительное показание для проведения биопсии — снижение порогового уровня ПСА до 2,5 нг/мл. Во время проведения секстантной биопсии при уровне ПСА 2,5-4 нг/мл обнаружение рака простаты составляет 2-4%, но при расширенной методике биопсии (12-14 вколов) оно увеличивается до 22-27%. Следует отметить, что в 20% случаев обнаруживают латентный рак (объем опухоли менее 0,2 см3). Таким образом, снижение верхней границы нормы ПСА ведёт к обнаружению клинически незначимых опухолей, которые и без лечения не угрожали бы жизни. Для того чтобы установить верхнюю границу нормы ПСА, позволяющую обнаружить непальпируемые, но клинически значимые опухоли, данных пока недостаточно. При определении относительных показаний необходимо учитывать и другие показатели ПСА (прирост, время удвоения и др.). Повышение верхней границы ПСА, при которой необходима биопсия, нерационально, поскольку сохраняется высокая вероятность обнаружения рака простаты. Лишь в возрасте старше 75 лег возможно повышение верхнего порогового значения до 6,5 нг/мл.
Прицельная биопсия предстательной железы необходима лишь при пальпируемой опухоли и уровне ПСА более 10 нг/мл. В целях уточнения диагноза при метастатическом или местнораспространённом процессе достаточно получения 4-6 биоптатов. В остальных случаях рекомендована множественная биопсия.
В последние 15 лет широкое распространение получила методика биопсии, предложенная К.К. Ходжем и соавт. (1989). Суть ее — во взятии биоптатов па середине расстояния между срединной бороздкой и латеральной границей предстательной железы из основания, средней части и верхушек обеих долей, в связи с чем методика получила название сектантной (6-точечной) биопсии. Метод 6-точечной биопсии в дальнейшем был усовершенствован таким образом, чтобы в биоптаты попадали заднебоковые отделы периферической зоны железы, которые недоступны при стандартной технике. Кроме того, с увеличением объёма предстательной железы частота обнаружения рака при использовании сектантной методики уменьшается. Необходимое число образцов ткани требует уточнения. Почти во всех исследованиях увеличение числа биоптатов повышало чувствительность метода (по сравнению с 6-точечной биопсией). Чувствительность биопсии тем выше, чем большее число биоптатов исследовано. В испытаниях на моделях железы установлено, что если объём опухоли составляет 2,5, 5 или 20% объёма железы, то при сектантной биопсии опухоль диагностируют в 36, 44 и 100% случаев. При выполнении биопсии следует учитывать, что в 80% случаев опухоль возникает в периферической зоне. По данным одного из исследований, взятие 13-18 биоптатов увеличивало чувствительность метода на 35%. В нормограммах Viеnnа (2003) отражена зависимость между количеством вколов, возрастом пациента и объемом простаты. При этом точность прогноза составляет 90%.
Зависимость количества биоптатов от возраста пациента и объёма простаты с точностью положительного предсказывающего прогноза 90%
|
Возраст, годы |
Объём простаты, мл |
|||
|
<50 |
50-60 |
70 |
>70 |
|
|
20-29 |
6 |
8 |
8 |
8 |
|
30-39 |
6 |
8 |
10 |
12 |
|
40-49 |
8 |
10 |
12 |
14 |
|
50-59 |
10 |
12 |
14 |
16 |
|
69 |
12 |
14 |
16 |
— |
|
>70 |
14 |
16 |
18 |
— |
Доказано, что при первичной биопсии захватывать переходную зону железы нецелесообразно, поскольку рак в ней встречают очень редко (менее чем в 2% случаев). В настоящее время наиболее распространена 12-точечная биопсия. Огромное значение придают не только количеству вколов, но и наклону иглы.
Заключение биопсии при раке простаты
В гистологическом заключении обязательно должны быть отражены следующие позиции:
- локализация биоптатов; особенно важна при планировании радикальной простатэктомии; распространенность опухоли на одну или обе доли учитывают при выполнении нервосберегающей операции; при поражении верхушки железы этап её мобилизации более сложен; высока вероятность положительного хирургического края при выделении сфинктера уретры;
- ориентация биоптата по отношению к капсуле железы; для уточнения дистальный (ректальный) отрезок окрашивают специальным раствором;
- наличие ПИН;
- объём поражения биоптата и количество положительных вколов;
- дифференцировка опухолевых клеток по Глисону;
- экстракапсулярная экстензия — обнаружение в биоптатах капсулы предстательной железы, прилежащей жировой клетчатки и прорастающей опухолевой ткани, что важно для выбора метода лечения;
- периневральная инвазия, указывающая на распространение опухоли за пределы предстательной железы с вероятностью 96%;
- сосудистая инвазия;
- другие гистологические изменения (воспаление, гиперплазия предстательной железы).
Если вышеперечисленные показатели не отражены в гистологическом заключении, то в нём обязательно следует указать расположение и количество положительных биоптатов, а также степень дифференцировки опухоли по Глисону.

Интерпретация данных биопсии при раке предстательной железы
Интерпретация данных биопсии требует индивидуального подхода. При отрицательном результате первой биопсии необходима повторная биопсия, вероятность обнаружения рака при этом составляет 10-35%. При тяжелой дисплазии вероятность обнаружения рака достигает 50-100%. В этом случае обязательно проведение повторной биопсии в ближайшие 3-6 мес. Доказано, что две биопсии позволяют обнаружить большинство клинически значимых опухолей. Даже после взятия большого количества биоптатов и отрицательном результате первой биопсии повторная биопсия достаточно часто обнаруживает рак. При подозрении на РПЖ ни один из методов диагностики не обеспечивает достаточной чувствительности, позволяющей отказаться от повторной биопсии. Случаи обнаружения единичного очага требуют особого внимания. Клинически незначимый рак (объём опухоли менее 0,5 см3) после радикальной простатэктомии наблюдают в 6-41% наблюдений. В данной ситуации следует комплексно оценить клиническую ситуацию и определить тактику лечения. Наиболее важную роль играют возраст пациента, уровень ПСА, степень дифференцировки опухоли, объём поражения биоптата, клиническая стадия. Наличие в биоптатах простатической интраэпителиальной неоплазии (ПИН) высокой степени (high grade) может свидетельствовать о злокачественном процессе в предстательной железе. Таким больным показана повторная биопсия через 3-12 мес, особенно если первоначально было получено 6 биоптатов. Показания к повторной биопсии — пальпируемое образование в предстательной железе, повышение уровня ПСА и тяжёлая дисплазия при первой биопсии.
К кому обратиться?
Диагностика рака предстательной железы
Статьи
| »» Содержание |
Б.П. Матвеев, Б.В. Бухаркин, В.Б. Матвеев |
Глава 4. Диагностика рака предстательной железы
Тщательно собранный анамнез помогает установить некоторые особенности заболевания. Симптомы рака предстательной железы, особенно дизурия, развиваются быстро. Иногда постепенно ухудшается общее состояние, больной жалуется на слабость, похудание. Внешний вид пациента изменяется только при далеко зашедшем опухолевом процессе. Истощение и выраженная бледность кожи наблюдаются редко. При осмотре следует обращать внимание на состояние лимфатических узлов, печени, почек, мочевого пузыря, определять количество остаточной мочи. При возникновении подозрения на рак предстательной железы в первую очередь принято проводить три необходимых исследования:
I. Пальцевое исследование простаты.
II. Определение уровня простато-специфического антигена (ПСА).
III. Ультразвуковое исследование (УЗИ) простаты, при показаниях -одновременно с биопсией.
Пальцевое исследование прямой кишки. Пальцевое исследование прямой кишки — самый простой, дешевый и безопасный метод диагностики рака предстательной железы. Однако результаты исследования во многом определяются размерами опухоли и ее локализацией. Пальпация железы осуществляется в коленно-локтевом положении больного, либо при лежании на правом боку. В результате пальпации врач может выявить следующие симптомы опухоли предстательной железы.
1. Ассиметричная предстательная железа.
2. Плотной или деревянистой консистенции части предстательной железы. Плотность может определяться в виде отдельных узлов, либо различной величины инфильтратов, вплоть до перехода их на стенки таза.
3. Неподвижность железы вследствие сращения ее с окружающими тканями.
4. Пальпируемые семенные пузырьки.
Данные, полученные при пальпации, не всегда легко интерпретировать, так как ложно положительный диагноз рака предстательной железы возможно поставить при следующих обстоятельствах:
1. Доброкачественная гиперплазия предстательной железы.
2. Камни предстательной железы.
3. Простатит.
4. Флеболиты стенки прямой кишки.
5. Полипы или рак прямой кишки.
6. Аномалии семенных пузырьков.
Результаты пальпации безусловно очень трудно дифференцировать от перечисленных заболеваний, но зато они являются вескими основаниями для дальнейшего обследования больного. В среднем только у одной трети случаев пальпируемых узлов предстательной железы впоследствии гистологически верифицируют рак простаты.
Определение уровня простато-специфического антигена (ПСА). Поскольку простато-специфический антиген имеет большое значение не только для диагностики, но и для лечения и прогноза рака предстательной железы, более подробно остановимся на этом маркере.
В скрининговых программах традиционно используют пороговый уровень в 4 нг/мл для всех возрастных групп. Использование предложенного уровня снижает количество ложно-положительных определений при гиперплазии предстательной железы.
Уровень ПСА в сыворотке крови может быть повышен по следующим причинам:
— рак простаты,
— доброкачественная гиперплазия простаты,
— наличие воспаления или инфекции в простате,
— ишемия или инфаркт простаты,
— эякуляция накануне исследования.
Диагностическая значимость почти всех опухолевых маркеров ограничена из-за ложно-положительных значений, наблюдаемых при некоторых незлокачественных патологиях. Длительно ведутся споры о том, оказывает ли пальпаторное обследование предстательной железы влияние на уровень ПСА в сыворотке. Некоторые авторы (Brawer et аl., 1988) считают, что такого влияния практически нет, другие наблюдали значительные изменения в уровне маркера после массажа простаты, хотя и не во всех случаях (Stamey et аl., 1987). С другой стороны, несомненно, инвазивные методы (трансуретральная биопсия или трансуретральная резекция простаты) приводят к значительному повышению сывороточного уровня ПСА. Stamey с соавторами (1987) в детальном исследовании показали, что при массаже простаты концентрация ПСА в сыворотке крови через 5 минут увеличивалась в 1.5-2 раза, и наиболее высокой была у больных с клиническими признаками гипертрофии. У больных, у которых массаж комбинировался с цистоскопией, ПСА увеличивался в 4 раза, а сразу же после биопсии перинеальных лимфоузлов и трансуретральной резекции — в 50-60 раз.
Из незлокачественной патологии предстательной железы простатиты острые или хронические могут приводить к значительному повышению ПСА (Dalton et аl., 1989). Доброкачественные гиперплазии могут давать высокую частоту ложно-положительных результатов, причем экспрессия антигена зависит от величины железы (Eicoreetal., 1987; Hudson et аl., 1989). Так Stamey с соавторами (1987) показали, что уровень ПСА у группы больных с гиперплазией предстательной железы перед операцией варьировал от 0.3 до 37 нг/мл и превышал уровень в 2.5 нг/мл у 86% тех больных, у которых вес резицированной ткани был от 6 до 36 грамм. Подсчитано, что концентрация ПСА в сыворотке больных с гиперплазией предстательной железы составляет 0.31 -0.2 нг/г гипертрофированной ткани. Частота ложноположительных значений при гиперплазии предстательной железы при пороговом уровне 4нг/мл по данным литературы колеблется от 20 до 55%.(Armitage et аl., 1988; Lange et аl., 1986; Hudson et аl., 1989). Другие авторы утверждают, что высокие значения ПСА при доброкачественных новообразованиях предстательной железы не так уж и редки.
Однако наибольшее значение определения ПСА безусловно имеет для диагностики рака предстательной железы. Следует отметить, что из трех основных исследований: определения ПСА, ректального и ультразвукового исследования предстательной железы — определение простато-специфического антигена имеет наименьшее количество ложноoтрицательных результатов и наибольшую специфичность. Серийный скрининг с применением ПСА в 2 раза увеличивает долю диагностики рака простаты в стадии Т1-Т2, в то время как пальцевое ректальное исследование выявляет лишь 30% гистологически подтвержденного рака той же стадии. До 90% рака простаты, выявляемого с помощью определения ПСА, приходится на поздние стадии заболевания. Чувствительность метода недостаточна для определения латентного, фокального, высокодифференцированного рака простаты. Так, Oesterling J. (1993) установил, что 20-40% всех злокачественных новообразований предстательной железы сопровождаются нормальной концентрацией ПСА в сыворотке крови. В то же время этот показатель при Т3-Т4 стадиях заболевания бывает положительным почти в 100% случаев.
При сравнении предоперационных уровней ПСА с результатами, полученными после простатэктомии, многие авторы отмечают высокую чувствительность и четкую корреляцию со стадией заболевания. Так из ряда работ (Stamey et аl., 1987, 1989), создается впечатление, что концентрация ПСА в сыворотке нелеченных больных пропорциональна объему опухоли в ткани простаты. Несмотря на определенную вариабильность предоперационных уровней ПСА у больных с клиническими стадиями А и В, показано, что его уровни ниже 15 нг/мл и выше 40 нг/мл являются достаточно четкими признаками отсутствия или наличия пенетрации капсулы, инвазии в семенные пузырьки и метастазов в тазовые лимфоузлы, хотя и при уровнях ПСА 15 нг/мл иногда возможна инвазия в капсулу железы.
Увеличение уровня ПСА до больших значений (около 20 нг/мл и выше) является высокоспецифичным даже при нормальных показателях ректального пальцевого исследования простаты. Поэтому при высоких цифрах ПСА биопсия предстательной железы должна проводится обязательно. Уровень ПСА более 50 нг/мл указывает на экстракапсулярную инвазию в 80% случаев и поражение регионарных лимфатических узлов у 66% больных (Stanley et аl., 1990). Исследования Rana et аl. (1992) показали, что результаты ПСА более 100 нг/мл указывают на 100% метастазирование (регионарное или отдаленное).
Наибольшие трудности возникают при интерпретации значений ПСА в диапазоне от 4 нг/мл до 20 нг/мл. Проведенные исследования свидетельствуют о том, что частота рака простаты у пациентов с концентрацией общего ПСА от 4 до 15 нг/мл и нормальными данными при пальцевом ректальном исследовании простаты достигает по разным данным от 27 до 37%.
Основным для клиницистов является осознание возможности выявления с помощью ПСА субклинических форм рака простаты без признаков экстра-капсулярной инвазии (стадии Т1 и Т2), когда возможно выполнение радикальной простатэктомии. По данным Myrtle et аl. (1986) показатели ПСА в сыворотке более 4 нг/мл наблюдались у 63% больных раком простаты стадии Т1 и у 71% — стадии Т2. В то же время, при экстракапсулярных поражениях (стадии Т3 и Т4) повышение ПСА наблюдалось в 88% случаев. В данной ситуации с целью более точной интерпретации повышенных значений общего ПСА весьма желательно исследование концентрации свободного ПСА и расчет соотношения «свободный ПСА/общий ПСА».
Помимо первичной диагностики рака простаты, определение ПСА широко применятся в следующих случаях:
1. После радикальной простатэктомии через несколько недель ПСА перестает определяться. Регулярные контрольные исследования (каждые 3 месяца) позволяют своевременно выявить рецидив заболевания в случае повышения ПСА. Если же показатели ПСА нормальны и нет клинических симптомов болезни, то исключаются другие исследования.
2. У больных, получавших лучевую терапию, отмечается значительное снижение уровня ПСА в сыворотке крови, что свидетельствует об эффективном лечении. В то же время, повышение ПСА говорит о малой чувствительности опухоли к проводимому лечению, либо о рецидиве заболевания. Следует отметить, что снижение ПСА до нормальных цифр коррелирует с уровнем антигена до лечения. Пациенты с показателями ПСА до лечения неболее 20 нг/мл имели нормальные показатели ПСА после лечения в 82% случаев. В то же время, у больных с более высокими цифрами ПСА до лечения этот процент составлял лишь 30%. Большинство пациентов со стабильным снижением ПСА оставались в ремиссии в течение последующих 3-5 лет.
3. Целесообразно определять ПСА у больных, получающих терапию антиандрогенами. Повышение уровня ПСА говорит о прогрессировании заболевания и о необходимости сменить характер лечения.
При антиандрогенном лечении уровень ПСА в сыворотке крови является точным индикатором успеха или неуспеха терапии. После начала терапии уровень ПСА быстро снижается у 50% больных (от 85 до 2.1 нг/мл), в то время как в отсутствие ответа величина ПСА не изменяется (Hudson et аl., 1989). Прогрессирование болезни наблюдалось в 50% случаев, когда уровень ПСА не снижался ниже 10 нг/мл. Это означает, что уровень ПСА не играет прогностического значения до начала терапии, в то время как в процессе лечения ПСА является хорошим индикатором эффективности терапии и хорошо коррелируется, как с выживаемостью, так и с длительностью ремиссии. Согласно Stainey (1989), повышение уровня ПСА через 6 месяцев после начала терапии может служить в качестве оценки чувствительности к проводимой терапии.
Ультразвуковая диагностика рака предстательной железы. Ультразвуковое исследование нашло очень широкое применение в диагностике многих заболеваний предстательной железы, в том числе и рака. Особенно интерес к исследованию проявился с введением трансректальной ультразвуковой томографии. Современные трансректальные ультразвуковые датчики обеспечивают очень высокое качество изображения и позволяют детально визуализировать структуру простаты, окружающих ее органов и тканей, а также прицельно взять биопсию из измененного участка железы. В норме неизмененная предстательная железа при ультразвуковом исследовании имеет треугольную форму. Основание железы обращено к прямой кишке, а верхушка — к шейке мочевого пузыря. Наибольший размер железы в поперечном направлении составляет 40-45 мм, в передне-заднем направлений он равен 20-27 мм, в продольном — 35-45 мм. На ультразвуковых томограммах различаются центральная и периферическая зоны простаты, которые обычно занимают большую часть предстательной железы. При ультразвуковом исследовании периферическая зона имеет однородную структуру и характеризуется отражениями средней интенсивности. Центральная зона расположена вокруг простатического отдела уретры, имеет ячеистую структуру, а по эхогенности ниже периферической зоны. При осмотре области шейки мочевого пузыря выделяется гипоэхогенная фибро-маскулярная строма, не содержащая желез, которая формирует переднюю часть простаты. Как считает В.Н. Шолохов (1997), с возрастом при развитии доброкачественной гиперплазии или при воспалительных заболеваниях центральная и периферическая зоны железы могут не дифференцироваться. Простатический отдел уретры выглядит в виде гипоэхогенного тяжа, проходящего в черную центральную зону железы.
Простата окружена перипростатической жировой клетчаткой и фасцией, которые формируют гиперэхогенный пограничный слой, который часто описывается как капсула железы. Истинная капсула простаты, если ее удается визуализировать, определяется в виде очень тонкой гипоэхогенной прерывистой линии по поверхности железы.
Семенные пузырьки визуализируются в виде симметричных гипоэхогенных тяжей, расположенных между простатой и мочевым пузырем размерами 2 х 7 см.
Как уже отмечалось выше, рак чаще всего развивается в периферической зоне простаты. Учитывая эту особенность, проще проводить дифференциальную диагностику с другими заболеваниями. Выявляемые структурные изменения, локализирующиеся в пределах центральной зоны, с большей вероятностью могут быть отнесены к проявлению доброкачественного процесса, в то время как обнаружение структурной перестройки, локализующейся в периферической зоне, чаще соответствует злокачественной опухоли.
Периферическая зона занимает 75% объема простаты, и в этой части железы рак возникает в 80% случаев. Большей частью опухоль располагается на глубине 3-4 мм от пограничною слоя. Центральная зона занимает около 20% объема железы. В этой части простаты развивается только 5% злокачественных новообразований. Вокруг простатического отдела уретры располагается тонкий участок железистой ткани — так называемая переходная зона. В норме она практически не дифференцируется от центральной зоны и занимает всего 5% объема простаты. В переходной зоне рак развивается в 20% случаев (Шолохов В.Н., 1997).
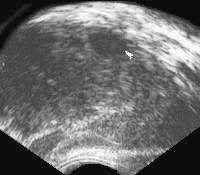
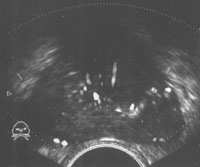
Наиболее характерными признаками рака простаты, локализующегося в периферической зоне, является наличие одного или нескольких узлов неправильной формы и пониженной эхогенности (рис. 4).
Рис. 4. Трансректальное исследование предстательной железы (продольная плоскость на границе периферической и переходной зоны), опухолевый узел (указан стрелкой) не выходящий за пределы органа. Признаков пенетрации капсулы нет.
Диагноз: рак предстательной железы.
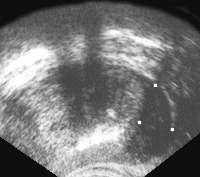
Нередко узел окружен гиперэхогенным ободком, что объясняется фиброзной реакцией соединительной ткани предстательной железы, окружающей опухолевый очаг. По мере роста опухоли появляются бугристые контуры железы с признаками пенетрации пограничного слоя (рис. 5 и рис. 6).
Рис. 5. Рак предстательной железы. Опухолевый узел в периферической зоне левой доли, инфильтрирует заднебоковую поверхность железы и перипростатической клетчатки.
Рис. 6. Трансректальное исследование предстательной железы (поперечная плоскость). Опухолевый узел в периферической зоне левой доли. Отмечается деформация наружного контура железы, признаки пенетрации собственной капсулы. (Т3) Диагноз: рак предстательной железы.
Особенно большое значение имеет выявление инфильтрации по передне-боковой поверхности железы, которая недоступна пальцевому исследованию.
Наиболее сложными для диагностики являются опухоли, которые локализуются в центральной и переходной зонах железы. Зачастую, развиваясь на фоне доброкачественной гиперплазии, рак по эхогенности практически не отличается от окружающих тканей, в связи с чем нередко возникают диагностические ошибки, а диагноз устанавливается при гистологическом исследовании удаленного материала во время операции.
По мере увеличения опухолевой инфильтрации стромы железы меняется ее ультразвуковая структура. Ткань железы становится неоднородной, с беспорядочными отражениями низкой интенсивности. Ультразвуковая томография позволяет выявить инфильтрацию капсулы простаты, семенных пузырьков мочевого пузыря, стенки прямой кишки, лимфатических узлов, что, естественно, позволяет уточнить стадию заболевания.
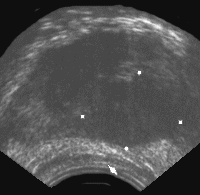
В отличие от рака, гиперплазия предстательной железы обычно развивается в переходной зоне по направлению к внутренней части железы. При этом переходная зона начинает сдавливать центральную и периферическую зону, вызывая их постепенную атрофию. Из центральной и периферической зон и фибромышечных слоев формируется «хирургическая капсула», по которой происходит «вылущивание» гиперплазированных узлов при операции. По мере роста доброкачественной гиперплазии железа приобретает шаровидную форму; при преимущественном росте периуретральных желез отмечается выбухание контура железы в просвет мочевого пузыря и формируется средняя доля, которая растет, оттесняя кпереди и деформируя заднюю стенку мочевого пузыря, сдавливая в значительной степени простатическую уретру и шейку мочевого пузыря. Поскольку доброкачественная гиперплазия предстательной железы не характеризуется инфильтративным ростом, то капсула железы обычно четко прослеживается по периферии среза. Частыми находками при доброкачественной гиперплазии являются мелкие ретенционные кисты и кальцинаты, генез которых связан со сдавлением протоков железы гиперплазированной тканью; располагаются они чаще всего по т.н. хирургической капсуле. При ультразвуковом исследовании простаты порой возникает необходимость проводить дифференциальную диагностику с простатитом. Это вызвано тем, что пальпация предстательной железы при простатите иногда дает результаты, очень похожие на рак. Ультразвуковое исследование в стадии отека и инфильтрации железы выявляет: увеличение железы (рис. 7 и рис. 8), изменение ее формы (чаще шаровидная) и структуры. Снижается эхогенность железы, теряется эхографическая дифференциация железистых и фибромышечных зон.
Рис. 7. Трансректальное исследование предстательной железы (поперечная плоскость). Хронический простатит с участками кальцификации в железе.
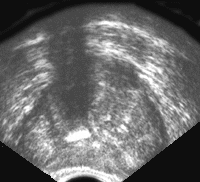
Рис. 8. Хронический простатит; усиление кровотока в ткани железы (режим энергетического Доплера).
При абсцедировании простатита — на фоне гипоэхогенной отечной ткани железы появляются анэхогенные зоны, соответствующие зонам некротических изменений. Постепенно происходит формирование стенки абсцесса в виде кистозной структуры с толстой стенкой и жидкостным неоднородным содержимым . При хроническом простатите эхоструктура железы может быть практически не изменена, либо выявляются диффузные повышенной эхогенности структуры в результате клеточной инфильтрации и склеротических изменений. Определяются кальцинаты и мелкие ретенционные кисты.
Описанные три основных метода диагностики в дальнейшем требуют обязательного морфологического подтверждения заболевания. С этой целью выполняется пункционная биопсия, которая наиболее достоверна при выполнении ее под контролем ультразвука. Особенно это касается обследования больных с малыми образованиями.
Биопсию предстательной железы можно производить через промежность, трансректально или трансуретральным доступом. Открытая биопсия применяется крайне редко. Трансуретральная резекция предстательной железы не только позволяет уточнить диагноз, но и обеспечивает восстановление мочеиспускания.
Трансвезикальная биопсия предстательной железы — вынужденная манипуляция у больных с подозреваемым раком предстательной железы, у которых в связи с острой задержкой мочеиспускания, обострением хронического пиелонефрита и высокой азотемией возникает срочная необходимость в проведении цистостомии.
В диагностике рака предстательной железы частота ложноотрицательных результатов гистологического анализа кусочков ткани при промежностном и трансректальном доступе не превышает 20%.
Осложнения пункционной биопсии встречаются крайне редко и могут быть связаны с повреждением мочевого пузыря и мочеиспускательного канала. Возможна гематурия, гематоспермия, промежностная и позадилобковая гематома. Для профилактики инфекционных осложнений, которые составляют около 2%, за сутки до биопсии и после нее назначают антибиотики.
В некоторых сложных случаях дифференциальной диагностики с успехом применяют цитологическую диагностику рака предстательной железы. Для цитологического исследования используют аспират из предстательной железы.
Цистоскопия является вспомогательным методом диагностики. При проведении цистоскопа может отмечаться девиация мочеиспускательного канала опухолевыми узлами. При цистоскопии удается обнаружить асимметричную деформацию шейки мочевого пузыря. В месте прорастания опухолью предстательной железы стенки мочевого пузыря определяется разрыхленность слизистой оболочки, фибриновые налеты, язвы или опухолевые разрастания, при этом трудно решить — прорастает ли опухоль из предстательной железы в мочевой пузырь или опухоль пузыря в железу.
Из методов диагностики рака предстательной железы заслуживает внимания рентгеновская компьютерная и магнитно-резонансная томография. Получаемая при этом информация соответствует таковой при ультразвуковом исследовании. На томограммах также видны структура предстательной железы, опухолевые узлы, их величина, степень прорастания капсулы, инфильтрация мочевого пузыря, семенных пузырьков, окружающей клетчатки. Эти методы, однако, оказались не более точными, чем трансректальное УЗИ при определении стадии ограниченного местного роста рака предстательной железы, и, более того, есть данные, что трансректальное ультразвуковое исследование дает более надежные результаты при оценке стадии заболевания.
Экскреторная урография позволяет оценить функцию почек и уродинамику верхних мочевых путей. Уретероэктазия и уретерогидронефроз являются следствием сдавления тазовых отделов мочеточников опухолью. Такие изменения часто бывают односторонними. При полной обструкции мочеточника происходит выключение почки, при этом тень рентгеноконтрастного вещества на стороне сдавления отсутствует.
Определение стадии заболевания. За установлением диагноза рака предстательной железы одновременно встает вопрос об установлении стадии заболевания, что в конце концов определяет характер будущего лечения. Кратко остановимся на возможностях применяемых методов исследования в установлении стадии заболевания.
Пальцевое исследование прямой кишки. Точность диагностики рака предстательной железы при пальцевом исследовании прямой кишки составляет 30-50%. Часто наблюдается недооценка стадии, поскольку небольшие, расположенные в передних отделах железы опухоли, как правило, не пальпируются; ложноположительные результаты наблюдаются у больных с гиперплазией предстательной железы и простатитом. Этот метод однако позволяет выявить рак предстательной железы, когда уровни ПСА остаются в пределах нормы, и предоставляют хотя не точные, но полезные данные о стадии заболевания. Пальпируемый неподвижный опухолевый инфильтрат или прорастание в кишку говорят о далеко зашедшем опухолевом процессе (Т4).
Определение простатического специфического антигена. При оценке отмечается достаточно четкая корреляция между уровнями ПСА и гистологической (и в меньшей степени клинической) стадией рака предстательной железы. У каждого конкретного больного корреляция не столь сильна из-за значительного перекрывания пределов различных возрастных норм. Уровни 10-20 нг/мл часто являются показателем опухоли, прорастающей за пределы капсулы предстательной железы, уровни выше 40 нг/мл свидетельствуют о наличии метастазов.
Хотя сывороточные уровни ПСА сами по себе не являются надежным показателем стадии заболевания, их можно использовать, чтобы избежать некоторых исследований. Выдвинуто предположение, что больным с вновь выявленным раком предстательной железы без симптомов поражения костей и при уровнях ПСА не выше 10 нг/мл не требуется проводить сцинтиграфию костей для определения стадии. У таких больных вероятность метастазов в костях приближается к нулю, хотя многие практические врачи считают этот метод исследования основным, так как при его помощи можно диагностировать «горячие точки», как например, остеоартроз позвоночника, который позже может создать путаницу в оценке симптомов. По данным Walsh et Partin (1994) при предоперационном ПСА < 4нг/мл и при сроке наблюдения 4 года у 92% больных не наблюдалось биохимического рецидива. При ПСА 4-10 нг/мл рецидива не было у 83% больных. При ПСА 10-20 нг/мл биохимического рецидива не было у 56%. И при ПСА > 20нг/мл рецидива не было только у 45%.
Казалось бы приведенные цифры убедительно показывают значимость ПСА для прогноза заболевания, но тем не менее надо принимать во внимание и другие исследования. По данным Элиса (1994) у 21% больных с ПСА < 4нг/мл был обнаружен рак, т.е., ПСА не является надежным критерием для установления стадии заболевания. На настоящий момент можно ориентироваться на следующие показатели ПСА. При ПСА свыше 40 нг/мл вероятность наличия метастазов в лимфатических узлах достигает 50%, поэтому выполнение тазовой лимфаденэктомии становиться необходимым. При ПСА < 10 нг/мл у нелеченных больных и показателе Глисона < 7 тазовая лимфаденэктомия может не выполняться.
Последнее время все чаще стали говорить об использовании ПСА в совокупности с показателем Глисона и пальцевого исследования простаты для диагностики лимфогенных метастазов. Например, если у больного определена клиническая стадия Т2а и число баллов Глисона — 3, при уровне ПСА 6 нг/мл ему не показана двусторонняя биопсия тазовых лимфоузлов для определения стадии, поскольку в этом случае вероятность метастазов в тазовых лимфоузлах приближается к нулю. Таким образом, ПСА — это ценный метод, который используется для оценки стадии в случаях вновь выявленного рака предстательной железы.
Ультразвуковое исследование предстательной железы. Возможности обычной трансабдоминальной эхографии ограничены: можно определить размеры железы, состояние капсулы, симметрию железы, объем остаточной мочи, однако выявление тонких изменений внутренней структуры железы и характера патологических изменений возможно только при поведении трасректального ультразвукового исследования.
При УЗИ основным диагностическим параметром является снижение эхогенности, но то же самое наблюдается и при других заболеваниях. Поэтому вероятность ошибки в установлении диагноза и соответственно стадии заболевания велика, особенно при небольших опухолях. Специфичность при диагностике рака предстательной железы составляет в среднем 20-30%.
Поиск метастазов при раке предстательной железы направлен на исследование регионарных лимфатических узлов и костей, где в первую очередь определяются метастазы. Диагностика лимфогенных метастазов в малом тазу сложна и имеется большая вероятность допущения ошибки (50-60%) даже при применении всех современных методов диагностики. Ультразвуковое исследование, рентгеновская компьютерная томография, магнитно-резонансовая томография — могут выявить метастазы, когда размер их превышает 2 см в диаметре, однако эти методы диагностики не позволяют обнаружить мелкие и микроскопические метастазы. Следует при этом отметить и то, что выявляемые увеличенные лимфатические узлы далеко не всегда поражены метастазами и при гистологическом исследовании находят только их гиперплазию.
Самая надежная информация получается после тазовой лимфаденэктомии, которая выполняется либо во время операции простатэктомии, либо как самостоятельное вмешательство.
Согласно Щуберту Е. и Венерту Е. (1985), путем тазовой лимфаденэктомии авторы выявили высокую частоту микрометастазов в тазовые лимфоузлы, которые не выявляются традиционными методами исследования. При этом гистологическое строение метастазов в лимфоузлах не всегда соответствовало строению первичной опухоли. Этим обуславливается необходимость лимфаденэктомии с гистологическим исследованием лимфоузлов методом ступенчатых срезов.
В последние годы тазовая лимфаденэктомия выполняется эндоскопически.
Сцинтиграфию костей, как правило, выполняют в случае вновь выявленного рака предстательной железы для оценки исходного состояния. Однако это метод при стандартном обследовании стали использовать реже, так как было доказано, что уровни ПСА являются более надежным диагностическим критерием при метастазах в кости; кроме того, последний метод дешевле. Таким образом, в 50% случаев рака предстательной железы при уровнях ПСА ниже 20 нг/мл сцинтиграфия костей считается не показанной.
Характерные изменения определяют при рентгенографии костей таза и поясничного отдела позвоночника, при их местатическом поражении, которые носят чаще остеобластический, реже остеолитический или смешанный характер. Вследствие чередования остеобластических и остеолитических участков, кости таза имеют пятнистый, мраморный вид.
Несмотря на применение всех современных методов диагностики рака предстательной железы все же допускается большой процент ошибок в установлении стадии заболевания. Как видно из приведенной таблицы 15 (данные Цинке, 1994), из 3170 больных правильное стадирование было только у 1497 больных (47%), после операции установлена стадия рТ3 у 1339 больных (42%) , метастазы в лимфатические узлы у 334 больных (11%), и опухоль по линии разреза была выявлена у 770 (24%) больных. В основном ошибки допускались в клиническх стадиях Т2b и с. Хотя ошибки были и при опухоли размерами Т1а и б. В большом проценте случаев клинически имеется занижение стадии болезни. Необходимо тщательное и полное предоперационное обследование. Тем не менее:
1) точное стадирование рака предстательной железы до операции ограничено;
2) у 20% больных с дооперационной стадией Т1а при гистологическом исследовании обнаруживают опухоль более 1 см3;
3) у 26% больных с дооперационным стадированием Т1б выявлена пенетрация капсулы, у 10% — инвазия семенных пузырьков;
4) у 37% больных с дооперационной стадией T1c найден распространенный рак (пенетрация капсулы), или опухоль по краю резекции, или инвазия семенных пузырьков, или наличие метастазов в регионарные лимфатические узлы).
Таблица 15. Ошибки клинического стадирования 3170 больных, подвергнутых радикальной простатэктомии по поводу клинически локализованного РПЖ (стадии Т2с и меньше) (Zincke et аl., 1994).
| Клиническая стадия | Число больных (%) | Паталогоанатомическая стадия | |||
| Ограничена предстательной железой | рТ3 | PN+ | Опухоль по линии резекции | ||
| Т1а | 49 (1.5%) | 44 (88%) | 4 (8%) | 1 (2%) | 2 (4%) |
| T1b | 177 (5,6%) | 120 (68%) | 46 (16%) | 11 (6%) | 35 (20%) |
| Т2а | 897 (28%) | 512 (57%) | 330 (37%) | 55 (6%) | 140 (16%) |
| T2b,с | 2047 (65%) | 82 (40%) | 959 (47%) | 267 (13%) | 593 (29%) |
| Всего: | 3170 (100%) | 1497 (47%) | 1339 (42%) | 334 (11%) | 770 (24%) |
Остановимся на значении степени дифференцировки опухоли и показателя Глисона. Каково их значение для решения вопроса о выборе метода лечения больного. Понятно, что целесообразность простатэктомии определяется:
1) наличие или отсутствие пенетрации опухолью капсулы простаты;
2) наличие опухоли по краю разреза;
3) по объему опухоли;
4) инвазия семенных пузырьков;
5) метастазы в лимфатических узлах.
При просмотре этих показателей у больных после простатэктомии в зависимости от показателей Глисона выяснилась прямая закономерность: чем меньше показатель Глисона, тем меньше вероятность большого распространения опухоли. И наоборот, чем больше показатель Глисона, тем больше вероятность распространения опухоли за пределы капсулы, тем больше вероятность рецидива опухоли (таб. 16).
Таблица 16. Корреляция между показателями Gleason и гистологическими данными простатэктомии.
| Гистологические данные | Gleason | |||
| 5 | 6 | 7 | 8-10 | |
| Пенетрация капсулы | 16% | 24% | 62% | 85% |
| Опухоль по краю разреза | 20% | 29% | 48% | 59% |
| Инвазия семенных пузырьков | 1% | 4% | 17% | 48% |
| Метастазы в лимфоузлы | 1% | 2% | 12% | 24% |
| Средний объем опухоли (см3) | 2.2 | 2.7 | 5.1 | 4 |
Так при показателе Глисона 8-10 пенетрация капсулы встречается чаще в 4 раза, чем при показателе 5, опухоль по краю разреза в 3 раза, объем опухоли больше в 2 раза, инвазия семенных пузырьков в 48 раз и метастазы в лимфатических узлах в 24 раза.
Исходя из приведенных данных можно сделать следующие выводы:
1. У больных с показателями Глисона 8-10 и метастазами в лимфатические узлы операция не целесообразна. Тем не менее, если больной все же оперируется с показателем Глисона 8-10 необходимо перед простатэктомией произвести срочное гистологическое исследование всех лимфатических узлов удаляемых во время тазовой лимфаденэктомии. При подтверждении метастазов простатэктомия не выполняется.
2. При показателе Глисона менее 8 лимфатические узлы можно исследовать в плановом порядке.
3. При показателе Глисона 7 больного следует оперировать.
4. При показателе Глисона менее 7 в зависимости от возраста, общего состояния больного можно наблюдать.
С целью подтверждения сказанного, в качестве примера, приведем данные Walsh (1993). Из 185 больных в стадии Т2, которым произведена простатэктомия — через 5 лет у 13% возникли рецидивы опухоли, а показатель Глисона у них был менее 7, в то время как у больных с показателем Глисона 7 прогрессирование опухоли отмечено у 59% больных.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Биопсия — самый «близкий к телу» метод диагностики. От пациента отщипывают кусочек и изучают под микроскопом. В воображении некоторых пациентов биопсия приравнивается чуть ли не к хирургической операции. Это не так, хотя и то, и другое может проводиться одновременно. Что же такое биопсия, какая она бывает и для чего проводится, рассказывает MedAboutMe.
Что такое биопсия в медицине?
Биопсия — это метод анализа тканей человеческого организма. Суть его очень проста: взять образец органа (биоптат), извлечь его из организма и внимательно рассмотреть. Собственно, сам термин это и означает в переводе с греческого: bios — живой и opsis — наблюдение при помощи глаз, то есть, визуальное исследование живой ткани.
История биопсии начинается с имени арабского врача Альбукасиса, которого называют мусульманским отцом хирургии — он же Абу аль-Касим Аль-Захрави. Именно он впервые использовал полую иглу, чтобы получить образец тканей зоба щитовидной железы и впоследствии исследовать его. Долгое время врачи делали биопсию, скорее, случайно, чем намеренно. Но в конце XIX века все изменилось. Технологии исследования тканей при помощи микроскопа и возможности взятия образцов развились достаточно — и медицина получила новый метод.
В России первую диагностику при помощи биопсии провел в 1875 году доктор М.М. Руднев. В 1878 году немецкие ученые описали исследование образца шейки матки. А в 1879 году парижский дерматолог Эрнест Анри Бенье, который проводил научные изыскания в области болезней кожи, ввел термин «биопсия», обозначив им процедуру взятия образцов тканей.
Следует понимать, что биопсия — это инвазивный метод, то есть, при этом совершается проникновение в тело человека. И это травматичный метод, приводящий хоть и к минимальным, но повреждениям тканей. Поэтому врачи назначают биопсию тогда, когда без нее не обойтись. Просто так данный метод никогда не используется.
Итак, биопсия позволяет получить образец клеток или тканей. Его можно изучать на клеточном уровне, то есть, исследуется состояние отдельных клеток и их компонентов — цитологическое исследование, для которого может использоваться световой или более мощный, электронный микроскоп. А можно при помощи светового микроскопа анализировать срез ткани — при многих заболеваниях изменения происходят в структуре ткани органа. Иногда при проведении гистологического анализа требуется предварительная обработка образцов специальными растворами — их окрашивание или иная подготовка для диагностики.
В зависимости от того, какой метод предполагается использовать, биопсия проводится разными путями.
Как получить образец для исследования при биопсии?
Для цитологического исследования образцы материала получают одним из следующих методов:
- Соскоб (мазок) — с пораженных тканей специальным шпателем или скальпелем на предметное стекло соскребается некоторое количество материала.
- Тонкоигольная биопсия — клетки органа или жидкость забираются путем отсасывания через полую длинную тонкую иглу. Так получают образцы костного мозга или кист.
При заборе кусочка тканей, в зависимости от того, какие ткани и каким образом надо исследовать, выделяют два вида биопсии:
- Эксцизионная — при этом удаляется и направляется на исследование все образование, а не отдельная его часть. Например, это может быть подозрительная родинка. В этом случае биопсия является одновременно и лечебной, и диагностической процедурой: сначала подозрительные ткани полностью удаляют, а потом проверяют: насколько они были опасны и не стоит ли поискать другие проявления болезни.
- Инцизионная — на исследование забирается только часть пораженной болезнью ткани.
Забор тканей может проводиться разными путями:
- Пункционная биопсия — образец тканей забирается при помощи полой иглы. Обычно используется для получения образца тканей, расположенных недалеко от поверхности кожи.
- Трепан-биопсия позволяет получать образец ткани в виде столбика при помощи трепана — специальной полой трубки. Используется при необходимости получения образца из плотных опухолей и костей.
- Кор-биопсия (режущая, сердцевинная биопсия) — разновидность трепан-биопсии, отличающаяся от нее механическими особенностями трепана. Проводится при помощи биопсийного пистолета — устройства для получения образцов молочной и щитовидной желез, почек, простаты, печени и других мягких тканей.
- Петлевая биопсия — при этом образец забирается при использовании петли и устройства, позволяющего резать ткань (коагулятор или радиочастотный аппарат). Проводят при эндоскопических исследованиях, а также при гинекологическом обследовании и др.
- Щипковая биопсия (панч-биопсия) — образец ткани удается получить при помощи специальных щипцов. Чаще всего используется при заболеваниях пищевод, желудка и кишечника.
- Скарификационная биопсия проводится устройством, позволяющим срезать тонкий слой ткани. Обычно используется при необходимости проведения биопсии кожи.
Самый частый побочный эффект биопсии — боль при проведении процедуры. Поэтому в большинстве случаев предварительно проводится местная анестезия — обезболивание конкретного участка, на котором будет проводиться забор тканей. Но, если речь идет только о соскобе, то, конечно, анестезия не нужна.
Биопсия не проводится при нарушениях свертываемости крови, а также при возможности получить требуемые данные другими, неинвазивными методами диагностики.
Биопсия и диагностика заболеваний
Устоялось мнение, что биопсия проводится, прежде всего, для опровержения или подтверждения предварительного диагноза «рак». И действительно, этот метод обязателен для окончательной постановки диагноза онкологами. Но он также успешно применяется и в других направлениях медицины, а не только в онкологии.
- Урологи исследуют ткани мочеполовой и мочевыделительных систем для поиска воспалительных процессов почек и мочевого пузыря, а также кистозных образований в них;
- Гинекологи при помощи биопсии диагностируют бесплодие, воспаление, предраковые состояния, а также некоторые эндокринные болезни;
- Гастроэнтерологи анализируют состояние желудочно-кишечного тракта: выявляют участки воспаления и ткани в предраковом состоянии и др.;
- Пункция лимфатических узлов проводится для их оценки при аутоиммунных, инфекционных и онкологических заболеваниях.
- Биопсия пересаженных органов необходима, чтобы проверить, не идет ли реакция отторжения.
- Пункция спермы может проводиться для оценки фертильности в ходе лечения бесплодия.
А в феврале этого года американские ученые сообщили, что разработали метод ранней диагностики болезни Паркинсона путем биопсии тканей подчелюстной слюнной железы. Метод позволяет выявить белок, указывающий на наличие болезни, на стадии, когда нет даже первых признаков заболевания. Это значит, что можно будет раньше начать лечение.
Обычно биопсия назначается, когда нет других возможностей получить информацию о клетках и тканях пораженного органа. Причем нередко забор тканей проводится «заодно» — раз уж все равно добрались до больного органа, почему бы не отщипнуть кусочек для анализа. То есть, взять образец тканей можно в процессе хирургической операции или других диагностических процедур, таких как:
- эндоскопия,
- колоноскопия,
- бронхоскопия и др.
Для проведения биопсии врач может воспользоваться дополнительным оборудованием, позволяющим наблюдать за процедурой, чтобы «не промахнуться» — томографом, аппаратом УЗИ или иной аппаратурой.
Ошибки при проведении биопсии
Идеальных методов диагностики медицина не знает. При проведении биопсии тоже возможны ошибки и получение ложноотрицательного результата, то есть, болезнь есть, но ее не нашли. Так, считается, что гистологическое исследование тканей — довольно точный метод и достоверен на 90%. Что может быть причиной ошибок при биопсии:
- при заборе было получено слишком мало материала и его оказалось недостаточно для полноценной диагностики;
- забор материала для анализа произведен не из опухоли, а из здоровых тканей рядом с ней;
- материал взят из зоны фиброза или некроза опухоли и не дает достаточно информации, чтобы определить наличие злокачественного образования;
- при подготовке материала к исследованию срез был проведен под неудачным углом;
- врач-морфолог не обладал достаточным опытом для выявления характерных признаков на сложном образце.
Выводы
- Биопсия — инвазивный, но малотравматичный метод диагностики, который никогда не назначается врачом просто так, без достаточных на то оснований. Если врач считает, что нужна биопсия — лучше не спорить, часто вовремя проведенный анализ является залогом жизни пациента.
- Современные технологии позволяют провести биопсию качественно и практически безболезненно.
- Результаты биопсии считаются окончательными. По ним врач может назначать лечение. Если результаты вызывают сомнения у врача (например, по всем признакам есть опухоль, а биопсия ее не показала) — возможна ошибка при заборе пробы. В этом случае врач может направить пациента на повторный анализ.
- Если результаты биопсии вызывают сомнения у пациента, он может забрать свои «стекла» с гистологическими срезами и отправить их на повторный анализ в другую клинику.
Клиническая лабораторная диагностика: национальное руководство / Под ред. В. В. Долгова, В. В. Меньшикова. – 2012
Руководство по лабораторным методам диагностики / Кишкун А.А. – 2013