Инсулин вводится подкожно. Вводить инсулин можно с помощью:
- инсулиновых шприцев;
- шприц-ручек;
- инъекционного порта (айпорта, iPort);
- инсулиновой помпы.
В Республике Беларусь инсулин чаще всего вводится с помощью инсулиновых шприцев.
Объемы инсулиновых шприцев: 0,3 мл, 0,5 мл и 1 мл. На шприц нанесены деления и цифры. Цифры означают количество единиц (от 10 до 100 ЕД). На картинке – шприц объемом 1 мл, в 1 мл – 100 ЕД, одно маленькое деление соответствует 2 ЕД инсулина.
Шприц должен соответствовать концентрации инсулина. Сейчас почти все инсулины с концентрацией 100 ЕД/мл и им соответствуют шприцы 0,1 мл – 10 ЕД (на шприце 1 мл маркировка 100 ЕД; 0,5 мл – 50 ЕД; 0,3 мл – 30 ЕД). Но раньше выпускался инсулин с концентрацией 40 ЕД/мл и для него существовали соответствующие шприцы (40 ЕД – 1 мл). Если в такой шприц набрать инсулин с концентрацией 100 ЕД/мл, то доза будет превышена в 2,5 раза. В нашей стране в настоящее время такие шприцы не выпускаются.
Кроме того, в аналоге инсулина туджео 300 ЕД в мл. Туджео вводится шприц-ручкой. Но если вдруг понадобится вводить туджео шприцем и набрать дозу инсулиновым шприцем на 100 ЕД/мл, то набранная доза будет больше нужной дозы в 3 раза.
Длина иглы в инсулиновом шприце от 6 до 13 мм. Толщина иглы обозначается буквой «G» (G31 – G26). Чем больше номер, тем тоньше игла (т.е. игла G31 будет тоньше, чем G26).
Выбор оптимальной длины и толщины иголки зависит от индивидуальных параметров организма и подбирается экспериментально.
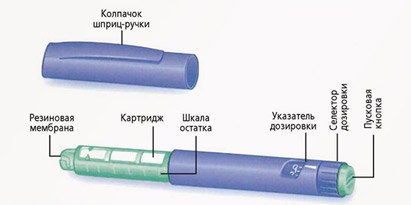
Шприц-ручки
Шприц ручка это устройство, в которое вставляется инсулин в специальных флаконах – картриджах. Устанавливается необходимая доза инсулина и вводится в виде инъекции (укола), как и шприцем. Иглы в шприц-ручках съемные и должны меняться после каждой инъекции инсулина. Иглы являются универсальными и подходят ко всем шприц-ручкам. После инъекции инсулина иглу надо снять. Нельзя хранить ручку с накрученной иглой. Из иглы может подтекать инсулин и в картридж может попадать воздух.
Иглы бывают длиной от 4 до 12 мм и толщиной G32 – G29. Как и в инсулиновом шприце, чем больше номер, тем тоньше игла.
Шприц-ручки бывают одноразовые и многоразовые.
Например, лантус выпускается в виде одноразовой ручки (Лантус СолоСтар) и в картриджах для многоразовой ручки (Лантус Пенфилл).
Одноразовая ручка содержит 300 ЕД инсулина (1 мл – 100 ЕД, в одной ручке 3 мл). Когда инсулин заканчивается, ручка выбрасывается. В многоразовых шприц-ручках вставляется инсулин в сменных картриджах. Один картридж (кроме Туджео) также содержит 300 ЕД инсулина (1 мл – 100 ЕД, 1 картридж – 3 мл). В Туджео в 1 мл содержится 300 ЕД.
В Республике Беларусь инсулин в картриджах выписывается только определенным категориям пациентов, указанным в приказе Минздрава (дети, беременные и др.).
Также ручки бывают электронными и механическими. Еще ручки отличаются по шагу, которым можно вводить инсулин (0,1 ЕД; 0,5 ЕД; 1 ЕД).
Для каждого инсулина – своя шприц-ручка!
Подробнее узнать о шприц-ручках можно на сайте www.test-poloska.ru.
Инъекционный порт
Смысл порта – сокращение количества инъекций. При его использовании выполняется 1 прокол при установке самого айпорта (специальным устройством под кожу вводится канюля), а далее укол инсулина делается не под кожу, а в резиновую мембрану айпорта. Инъекционный порт устанавливается на 72 часа или на 75 инъекций. Канюля айпорта бывает 6 и 9 мм (для детей – 6 мм, для взрослых – 9 мм). В айпорт нельзя одновременно вводить короткий и длинный инсулин. Разница между инъекциями должна быть не менее 60 минут. Причем сначала надо вводить короткий инсулин и только через 60 минут в айпорт можно ввести инсулин длительного действия. После введения в айпорт инсулина длительного действия ввести в него короткий инсулин можно не ранее чем через 3 часа. Поэтому часто инсулин короткого действия вводят в айпорт, а длительного – обычной инъекцией.
Инъекции в мембрану айпорта можно выполнять шприцами и ручками. Но иглы должны быть не менее 6 мм.
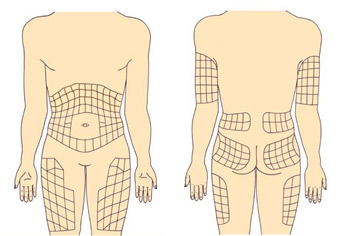
Рекомендуемые места введения инсулина
Инсулин можно вводить в область передненаружной поверхности бедер, ягодицы, наружную поверхность плеч, живот. В области живота инсулин не вводится вокруг зоны пупка (отступить 2 см по диаметру), в область срединной линии живота, от ребер вниз надо отступить 2 см.
В зависимости от того, куда ввели инсулин, отличается время действия генно-инженерного инсулина (аналогов это не касается). Самое быстрое действие инсулина наступает при введении в живот, поэтому в живот вводится инсулин короткого действия. Инсулин длительного действия вводится в бедра, ягодицы.
Вводить в плечи инсулин желательно, только если инъекцию выполняет кто-то другой.
Инсулин будет быстрее всасываться в условиях повышенного кровообращения (после бани, горячего душа, массажа места инъекции, физической нагрузки). Замедляет действие инсулин охлаждение, спазм сосудов, обезвоживание.
Нельзя вводить инсулин в одно и то же место, места введения инсулина необходимо чередовать (левое-правое бедро или плечо, левая – правая половина живота), расстояние между инъекциями инсулина должно быть не менее 2 см. Инсулин не вводится в область рубцов, стрий (растяжек).
Необходимо регулярно осматривать и прощупывать места инъекций. При неправильной технике инъекций (многократные инъекции в одно место, введение холодного инсулина, многократное использование игл и пр.) в местах введения инсулина могут образовываться уплотнения («шишки») – гипертрофическая липодистрофия. Реже в местах введения инсулина может происходить истончение подкожно-жировой клетчатки («впадины») – атрофическая липодистрофия. В места липодистрофий инсулин вводить нельзя! Если ввести инсулин в места липодистрофий, он не будет оказывать действия, также инсулин может там накапливаться и действовать непредсказуемо. В места липодистрофий теряется чувствительность, поэтому часто пациенты вводят туда инсулин, потому что там «небольно». Так делать нельзя.
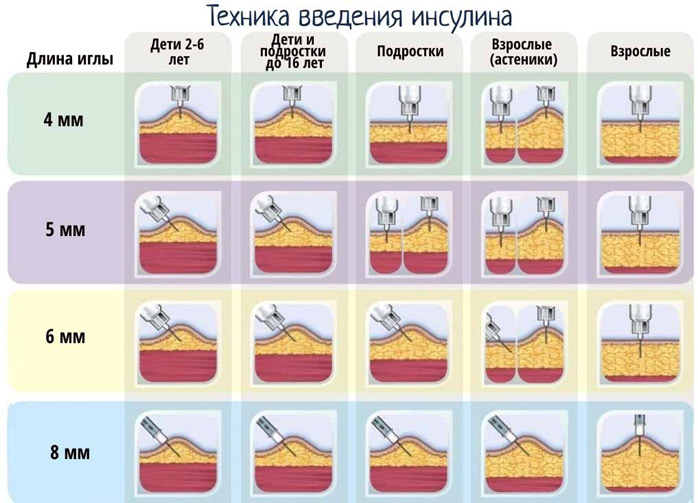
Техника введения инсулина
Если Вы вводите продленный НПХ-инсулин («мутный» длинный инсулин), то перед употреблением его надо перемешать, перекатывая между ладонями не менее 10 раз (нельзя трясти флакон).
Если инсулин вводится шприцем, то в шприц надо набрать воздух соответственно количеству единиц инсулина (если вводите 10 ЕД инсулина, необходимо набрать 10 ЕД воздуха). Затем ввести набранный воздух из шприца во флакон с инсулином и набрать нужное количество инсулина. Удалить пузырьки воздуха из шприца (иглу вверх, постучать по шприцу), выпустить из шприца лишний воздух и 0,5-1 ЕД инсулина.
Если инсулин вводится шприц-ручкой, то надо набрать и выпустить 0,5-1 ЕД инсулина, держа при этом ручку иглой вверх.
Инъекции выполняются на чистом участке кожи чистыми руками. Если Вы соблюдаете правила личной гигиены, ежедневно принимаете душ, нет необходимости дезинфицировать кожу перед каждым уколом.
Необходимо сформировать кожную складку (в складку нельзя захватывать мышцы, должна захватываться только кожа). Инъекции инсулина должны осуществляться в подкожный жир, а не внутрикожно или внутримышечно. Складку надо брать двумя пальцами, а не всей кистью (чтобы не захватить мышцы).
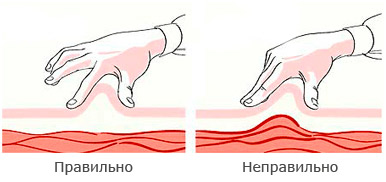
Игла вводится в зависимости от толщины подкожно-жировой клетчатки вводится под прямым углом или под углом 450 в основание складки, срезом иглы вверх.
После введения иглы надо плавно нажать на поршень шприца или шприц-ручки (шприц-ручку обхватить 4 пальцами, нажимать большим пальцем), ввести инсулин и удерживать шприц под кожей не менее 10 секунд (считать до 20). Чем больше доза, тем дольше надо держать иглу. После этого достать иглу (складку не отпускать!), подождать немного (досчитать до 3) и отпустить складку.
Хранение инсулина
Запас инсулина должен храниться в холодильнике при температуре от 2 до 80С. Инсулин нельзя замораживать! Если инсулин был заморожен, его нельзя использовать. В самолете инсулин нельзя сдавать в багаж, т.к. там он может замерзнуть.
Флакон, из которого вводится инсулин может храниться при комнатной температуре (до 250С) до 4 недель. Следует избегать попадания прямых солнечных лучей на инсулин.
Если инсулин достали из холодильника, он должен находиться при комнатной температуре не менее 1 часа.
В поездках, на пляже запас инсулина надо хранить в специальных термочехлах для хранения инсулина. Также термочехлы надо использовать при отрицательной температуре окружающего воздуха. При отрицательной температуре окружающего воздуха инсулин надо перевозить, положив его ближе к телу, а не в сумке.
Нельзя использовать инсулин при изменении цвета, появлении хлопьев, осадка.
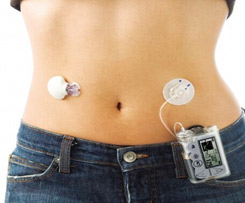
Инсулиновая помпа
Инсулиновая помпа представляет собой устройство, с помощью которого осуществляется постоянная подкожная инфузия инсулина. При этом вводится ультракороткий инсулин с заданной скоростью в качестве базального инсулина и дополнительно вводятся болюсы инсулина на еду.
При этом можно изменять скорость введения базального инсулина по часам (эффективно при синдроме утренней зари), применять различные болюсы введения короткого инсулина (эффективно для компенсации различной еды). Помпа не заменяет мониторинг глюкозы (мониторинг это одна статья расходов, помпа – другая). Также надо понимать, что помпа не является искусственной поджелудочной железой, решение о вводимых дозах инсулина принимает не помпа, а пациент. При использовании помпы надо уметь точно считать углеводы, знать свои коэффициенты. Помпу есть смысл ставить, когда имеется понятие о компенсации диабета. При отсутствии знаний помпа сама по себе не решит проблемы компенсации.
Существуют проводные и беспроводные помпы. В беспроводных помпах (Омнипод) инсулин находится в специальных устройствах (подах), которые устанавливаются на тело. Управление подачей инсулина осуществляется через специальный пульт. Цена одного пода – 20-25 $, один под устанавливается на 72 часа, на месяц нужно минимум 10 подов. Цена пульта составляет порядка 600 $.
В проводных помпах инсулин находится в специальном резервуаре в помпе. Помпа фиксируется на одежде, на теле подкожно устанавливается канюля (тефлоновая или стальная), инсулин подается от помпы к канюле через специальный катетер. Резервуар, канюлю и катетер надо менять каждые 3 дня.
В Республике Беларусь сертифицированы проводные помпы компании «Медтроник», которые продает компания Zarga, на сайте которой можно ознакомиться с действующими ценами.
Основные проблемы, которые возникают при использовании помпы:
- высокая стоимость (бесплатно помпы могут устанавливаться детям и беременным, инфузионные наборы покупаются пациентами за свой счет, инсулин бесплатно);
- неудобство при ношении, необходимость снятия на период водных процедур (душ, купание);
- загибы канюлей, вследствие чего инсулин перестает поступать в организм.
Сегодня расскажем о главных ошибках при использовании инсулиновых шприц-ручек, которые не стоит допускать.
По неопытности или невнимательности можно перепутать шприц-ручку с инсулином (ультра)короткого действия со шприц-ручкой с инсулином длительного действия. Во избежание подобного, старайтесь держать щприц-ручки разного назначения отдельно друг от друга и/или маркировать цветом (маркером или наклейкой).
Передача своей шприц-ручки для использования другому лицу. Шприц-ручка – средство для индивидуального использования. Даже если поменять иголку, риск передачи инфекционных заболеваний сохраняется.
Нарушение правил хранения инсулина. Запасы инсулина следует держать в холодильнике при температуре 2- 6°С. Шприц-ручку, которую используете, можно хранить при комнатной температуре не больше 1 месяца, вдали от источников тепла и солнечных лучей.
Избегайте нагревания и замораживания инсулина.
Нарушение техники инъекции инсулина: не забывайте менять места инъекций, каждый раз надевать новую иглу и заполнять ее инсулином (на 2ЕД) до появления капли, удерживать иглу под кожей не менее 6 секунд после введения инсулина.
Увеличение дозы инсулина длительного действия по причине высокого сахара крови перед сном. Базальный инсулин не предназначен для снижения сахара крови, он необходим для предотвращения повышения глюкозы крови натощак. Если у вас перед сном высокий сахар, сделайте подколку небольшой дозы инсулина ультракороткого действия и пересмотрите, правильно ли вы рассчитываете дозу инсулина на ужин.
При подсчете очередной дозы инсулина (ультра)короткого действия перед едой или «на снижение» гликемии забывают учитывать время, которое прошло с предыдущей инъекции инсулина. Если прошло менее 4 часов, в крови еще есть активный инсулин. Помните об этом при расчете очередной дозы инсулина (ультра)короткого действия — это позволит избежать гипогликемии.
Информация, представленная в материале, не является медицинской консультацией и не может заменить визит к врачу.
Статья посвящена оценке влияния техники инъекций на эффективность инсулинотерапии у пациентов с сахарным диабетом 2-го типа
Влияние техники инъекций на гликемический контроль
В исследованиях показано, что в зависимости от соблюдения правил инъекции результаты контроля гликемии могут отличаться на 10–50%.
В исследовании Nakatani Y. et al. [1] показано, что даже 10-минутное обучение пациентов технике инъекций инсулина снижает HbA1c на 0,7% (c 7,46% до 6,73%; p<0,01). Сохранность знаний после очередного обучения составляет 8–12 мес. [2], это дает возможность своевременно спланировать повторное обучение.
Связь уровня HbA1c и обучения технике инъекций исследуется наиболее часто [1, 3], однако техника инъекций влияет и на их болезненность (у 50,8% пациентов) [4], образование кровотечений и кровоподтеков, возникновение липодистрофий, соответствие фактически введенной дозы набранной [5].
Серьезной проблемой является то, что обучение технике инъекций в основном проводится в ходе рутинного приема врача, и бывает, к сожалению, крайне отрывочным и формальным.
Достаточно небольшой процент специалистов и пациентов пользуются разработанными в 2011 г. на основе международных рекомендаций Российскими национальными рекомендациями по технике инъекций [6, 7]. Отсутствие знаний по технике инъекций приводит к серьезным ошибкам, влияющим на эффективность инсулинотерапии. Так, в российской ветви международного исследования TITAN было показано, что 30,9% пациентов боятся инъекций инсулина при инициации терапии, 88% – используют длинные инсулиновые иглы, 19% инъекций в область живота и 29% инъекций в область бедра выполняются без формирования кожной складки, 55% пациентов отпускают складку раньше, чем вынимают иглу, 28% – не получали от врача информацию о глубине введения иглы под кожу, 40% – не получали от врача информацию о возможности индивидуального выбора длины иглы, 22% – не знают, что инъекции можно выполнять под углом 45°. Подобные результаты были получены исследователями из Китая: J. Ji et al. [3] показали, что 35,26% пациентов имели липогипертрофию, а 58,68% – кровотечения или кровоподтеки в местах инъекций, что свидетельствует о нарушении техники инъекций и статистически значимо коррелирует с повторным использованием игл для инъекций, инъекциями в одно и то же место и уровнем HbA1c. Для исправления данной ситуации необходимо применять качественную программу обучения пациентов. В Российских и международных рекомендациях предложена эффективная программа обучения со следующими обязательными компонентами [6–11]:
– режим выполнения инъекций;
– выбор и правильное применение устройств для инъекций;
– выбор, уход и самостоятельное обследование участков инъекций;
– правильная техника выполнения инъекций (чередование мест введения, выбор правильного угла наклона иглы, формирование кожных складок);
– осложнения при нарушении техники инъекций и способы их профилактики;
– выбор оптимальной длины иглы;
– надлежащая методика утилизации игл.
Внедрение подобных программ обучения технике инъекций пациентов приводит к значительному успеху. Наглядным примером является опыт китайских коллег: в 2009 г. 50% пациентов использовали иглы длиной 5 мм [12], а в 2014-м – уже 75% [4].
Помимо теоретического обучения технике инъекций и контроля знаний пациентов с помощью типовых опросников (выбор и смена места инъекции, формирование складки, угол наклона иглы, продолжительность инъекции, повторное использование игл, инъекции в область липодистрофий) крайне важным является контроль со стороны врача, включающий регулярный осмотр мест инъекций (контроль за вытеканием инсулина или крови, кровоподтеками, липодистрофиями, воспалением, болью) [13]. В таблице 1 представлены простые и четкие инструкции по выполнению инъекций инсулина.
Влияние техники инъекций на эффективность применения традиционных препаратов инсулина у пациентов с СД2
В нашей стране достаточно высокий процент пациентов (50% и более) с СД2 лечатся при помощи традиционных препаратов инсулина человека, поэтому очень важно обучить пациентов правилам работы с ними, чтобы повысить эффективность и безопасность терапии.
Оптимальное всасывание инсулина обеспечивается при его инъекции в подкожную жировую клетчатку. При несоблюдении правильной техники введения инсулина возможно его попадание в кожу или мышцу, что существенно отражается на эффективности действия препарата. Попадание инсулина внутрь кожи замедляет его всасывание, а также повышает риск развития аллергических реакций, в которых принимают участие клетки иммунной защиты, расположенные в коже [8, 9]. При попадании инсулина в мышцы его всасывание происходит значительно быстрее, чем из подкожной клетчатки, что чревато возникновением гипогликемии. Толщина кожи (эпидермиса и дермы) варьирует в диапазоне от 1,2 до 3,5 мм (рис. 1) в зависимости от места инъекции, возраста человека, расы и пола, что позволяет рекомендовать использование более коротких инсулиновых игл всем пациентам для предотвращения внутримышечного введения, которое может приводить к декомпенсации диабета и возникновению дефектов кожи и подкожно-жировой клетчатки. В то же время эффективность введения инсулина с помощью 4, 5, 6 мм игл является сопоставимой с эффективностью при использовании более длинных игл [14]. В настоящее время известно, что иглы, которые раньше рекомендовались для инъекций инсулина (для взрослых пациентов >8 мм, для детей >6 мм), являются слишком длинными и повышают риск внутримышечного введения. Более короткие иглы намного безопаснее, лучше переносятся и менее болезненны. В исследовании L. Hirsch et al. было продемонстрировано, что 4 мм игла является безопасной и эффективной у взрослых пациентов любого веса: все пациенты имели эквивалентный гликемический контроль, сопоставимое вытекание инсулина из кожи в сравнении с иглами 5 и 8 мм и при этом меньший уровень болевых ощущений [15].
Обеспечить точное введение инсулина в подкожно-жировую клетчатку возможно только при условии введения иглы в кожную складку, сформированную двумя пальцами – большим и указательным. В складку надо захватывать только кожу и клетчатку, но не подлежащую мышцу. Для наилучшего всасывания препарата рекомендуется удерживать складку в течение 10–15 с после окончания инъекции, продолжая давить на поршень шприц-ручки, чтобы все нужное количество инсулина успело вытечь из иглы. Если из места инъекции вытекает капля крови или инсулина, то в таком случае не нужно вводить дополнительно инсулин, т. к. это может привести к передозировке препарата и гипогликемии.
Для каждой области тела характерна своя скорость всасывания инсулина. Традиционные препараты инсулина, введенные в подкожную жировую клетчатку живота, всасываются быстрее, чем введенные в область бедра, соответственно возрастает и скорость снижения концентрации глюкозы в крови. В связи с этим существуют четкие инструкции: традиционные человеческие инсулины короткого действия рекомендуется вводить только в область живота, тогда как инъекции инсулинов пролонгированного действия лучше делать в область плеча, бедер или ягодиц. Всасывание инсулина из области ягодиц происходит быстрее, чем из области бедер, но медленнее, чем из области живота.
На скорость всасывания инсулина влияет температура в месте инъекции, поэтому ускорить действие инсулина, введенного «на еду», можно путем растирания места введения перед инъекцией и разминания этой области после укола. Физическая нагрузка также ускоряет всасывание инсулина, поэтому перед длительной прогулкой лучше ввести пролонгированный инсулин в область плеча.
Согласно исследованию Т. Heise et al. [16], причиной боли при подкожном введении инсулина является не скорость введения инсулина (отличие статистически незначимо), а объем (положительная связь) и место инъекции (рука или область живота). Эти сведения обосновывают рекомендацию «разбивать» большие дозы инсулина на несколько проводимых одномоментно в разные анатомические области инъекций.
В Национальных рекомендациях по технике инъекций изложены следующие правила работы с традиционными человеческими препаратами инсулина [6].
• Необходимо избегать внутримышечных инъекций инсулина короткого действия и НПХ-инсулина ввиду опасности развития выраженной гипогликемии.
• НПХ-инсулины имеют фармакологические пики, которые могут обусловливать развитие гипогликемии, особенно при введении относительно больших доз. Может быть целесообразно разделение больших доз инсулина на две инъекции. Нет универсальной пороговой величины для разделения доз, но, как правило, за нее принимают величину 40–50 ЕД.
• Бедра и ягодицы предпочтительны при использовании НПХ-инсулина в качестве базального инсулина, т. к. всасывание в этих местах самое медленное. По возможности НПХ-инсулин следует вводить перед сном, а не перед ужином, чтобы снизить риск ночной гипогликемии.
• Быстрее всего растворимые человеческие инсулины короткого действия всасываются при введении в область живота, поэтому их предпочтительно вводить именно в эту область.
• Всасывание растворимых человеческих инсулинов короткого действия у пожилых людей может быть замедленным, поэтому эти инсулины не следует использовать, когда необходим быстрый эффект.
• Учитывая различия в скорости всасывания человеческих инсулинов в разных областях, схема чередования мест инъекций должна быть одинаковой каждый день.
Параллельно с традиционными препаратами инсулина используются современные аналоги человеческого инсулина, применение которых неуклонно растет. Выполнено несколько исследований, непосредственно направленных на изучение оптимальных методик введения этих лекарственных средств.
• Для введения быстродействующих и смешанных аналогов инсулина можно использовать участки кожи любой локализации, поскольку они везде всасываются с одинаковой скоростью.
• Быстродействующие аналоги инсулина не следует вводить внутримышечно, хотя исследования демонстрируют, что жировая ткань и расслабленная мышца характеризуются схожей скоростью всасывания. Однако нужны исследования по изучению скорости всасывания из сокращающейся мышцы.
• Следует исключить внутримышечные инъекции аналогов инсулина длительного действия и смешанных аналогов ввиду опасности развития выраженной гипогликемии. Пациентов, занимающихся физическими упражнениями после инъекций длительно действующих аналогов инсулина, следует предупредить о возможном риске гипогликемии.
• Согласно полученным новым данным (FIT-2015) у базальных аналогов человеческого инсулина есть недостоверные различия в скорости всасывания. По-прежнему пролонгированные аналоги можно вводить в участки кожи любой локализации [17], однако гларгин немного медленнее всасывается из области живота в сравнении с областью бедра, а детемир, наоборот, медленнее всасывается из области бедра в сравнении с областью живота.
Влияние инъекций инсулина в область липодистрофий на гликемический контроль у пациентов с СД2
Нерешенной в настоящее время остается проблема липодистрофий (ЛД), поскольку не установлен их механизм развития. Липодистрофия – это нарушение состава жировой ткани. Существует два основных вида ЛД: липоатрофия означает потерю адипоцитов и клинически проявляется в виде образования «щербин» и «кратеров»; липогипертрофия (ЛГ) – это увеличение числа адипоцитов, которое проявляется развитием отека и/или уплотнения жировой ткани (рис. 2). Распространенность ЛГ остается высокой и варьирует в диапазоне 20–75%. В исследовании, проведенном испанскими специалистами, ЛГ отмечена у 53,4% пациентов с СД2. Наиболее изучена и доказана связь развития ЛГ с плохой ротацией мест инъекций [7]. Доступным решением этой проблемы является прекращение инъекций инсулина в области, где ЛГ уже возникла, при этом возможно исчезновение ЛГ. Скорость всасывания инсулина, введенного в ЛГ, непредсказуема. Это может привести к гипергликемии, гипогликемии или более высокой вариабельности уровня глюкозы, что достоверно ухудшит гликемический контроль и будет небезопасным для пациентов.
В исследовании Blanco M. et al. было установлено, что при введении инсулина в область ЛГ происходит увеличение эффективной дозы инсулина, что приводит к чрезмерной гиперинсулинизации пациента и неблагоприятно сказывается на его весе [18].
Частота использования инсулиновых игл с риском развития ЛГ является доказанной. В исследованиях продемонстрировано, что вероятность возникновения ЛГ составляет 75% при использовании 1 иглы более 4-х раз и 100% при замене иглы во время замены картриджа (табл. 2) [7].
Определенную роль в генезе ЛГ отводят иммунологическим факторам, зависящим от качества инсулина, особенно, его субстанции.
Под действием кристаллов инсулина и белковых примесей происходит локальная иммунная реакция. В ответ на воспаление начинается местная гиперпродукция фактора некроза опухоли α (TNF α) из макрофагов, что, в свою очередь, приводит к нарушению дифференцировки адипоцитов и развитию ЛГ.
В этой связи определенный интерес представляет качество субстанций, применяемых инсулинов в том числе отечественных, т.к. кол-во пациентов, получающих такие инсулины неуклонно растет. Преимущество собственного производства субстанции заключается в возможности установки более жестких режимов очистки от примесей, которые неизбежно возникают при генно-инженерной технологии получения инсулина.
Таким образом, на основании мирового опыта и отечественных данных можно сделать вывод, что правильность применения инсулина, назначенного врачом пациенту с СД2, играет огромную роль в эффективности и безопасности данного метода лечения. Огромное количество скрытых ошибок и проблем у пациентов с СД, получающих инсулин, обусловлены отсутствием знаний и навыков правильной техники инъекций [19].
Структурированное обучение пациентов позволит ликвидировать пробелы в образовании больного и достигнуть адекватного контроля инсулина.
Аннотация
Цель.
Оценить технические аспекты проведения инъекционной антигипергликемической терапии у пациентов с сахарным диабетом(СД) 1 и 2 типа.
Материалы и методы.
Выборку составили 200 взрослых пациентов (60 мужчин и 140 женщин), получавших инъекционную терапиюне менее 6 месяцев. Всем пациентам было предложено заполнить специально разработанный опросник, который состоял из 40 вопросов,направленных на оценку основных социо-демографических параметров, особенностей применения различных устройств для инъекций,а также выявление наиболее часто допускаемых пациентами ошибок.
Результаты.
Средний возраст пациентов составил 51,7?15,1 лет, средняя длительность заболевания — 11,9?9,1 лет. Средний уровеньHbA1c соответствовал 8,4?1,5%. В качестве устройства для инъекций 130 (65%) пациентов использовали полуавтоматические доза-торы — шприц-ручки, 39 (19,5%) — одноразовые шприцы, 31 (15,5%) — применяли одновременно оба вида инъекторов. Наиболее широкоиспользовались иглы длиной 8 мм, их применяли 122 (61%) обследованных больных; иглами длиной 12,7 мм пользовались 32 (16%) пациента,10 мм — 31 (15,5%), 12 мм — 28 (14%), 6 мм — 19 (9,5%) и 5 мм — 18 (9,0%) пациентов. При этом 64 (32%) человека осуществляли инъ-екции иглами разной длины, а 25 (12,5%) больных не смогли точно ответить на вопрос о длине используемых игл. Пациенты с разной ча-стотой использовали для введения инсулина различные анатомические области. 87 (43,5%) обследованных больных осуществлялиинъекции в пределах одной анатомической области: в 62 случаях в передне-брюшную стенку, 19 — в передне-боковую поверхность бедер,5 — в плечи, 1 — в ягодицы. В 113 (56,5%) случаях инъекции осуществлялись в две или более области тела. У 83 (41,5%) пациентов в местахинъекций имелись участки уплотнения, при этом 42 (50,6% из имевших участки липодистрофий) пациента продолжали осуществлятьинъекции в измененные участки, причем 12 из них делали это регулярно, 30 — эпизодически. Выявлены различия в уровне HbA1c у пациен-тов, использующих для инъекций места уплотнений, и тех, у кого не отмечалось изменений подкожной клетчатки — 9,5 и 8,2% соот-ветственно (р=0,02). Более половины опрошенных больных — 106 (53%) — получили информацию о технических вопросах подкожныхинъекций от своего эндокринолога; 60 (30%) пациентов были обучены средним медицинским персоналом в стационаре или эндокриноло-гическом диспансере, 28 (14,0%) получили знания во время занятий в школе диабета?, 9 (4,5%) — на приеме участкового терапевта,19 (9,5%) пациентов были обучены немедицинскими специалистами.
Заключение.
Значительное число пациентов допускают целый ряд серьезных ошибок, осуществляя инъекции инсулина. Несоблюдениеправил введения ассоциируется с ухудшением показателей углеводного обмена, в связи с чем технические вопросы инсулинотерапиидолжны находиться в центре внимания любого практикующего врача. Дается обзор новых международных рекомендаций по техникеинъекций, выпущенных в 2010 г.
Достижение и длительное поддержание компенсации углеводного обмена является одной из целей терапевтической тактики при сахарном диабете (СД). Значительная доля современных антигипергликемических средств представлена препаратами с инъекционным путем введения. В настоящее время к ним относятся инсулин, агонисты рецепторов глюкагоноподобного пептида-1 (ГПП-1) и аналоги амилина [1, 2]. Последнее десятилетие ознаменовано неуклонным ростом во всем мире числа пациентов с СД как на терапии препаратами инсулина и его аналогов, так и использующих агонисты рецепторов ГПП-1. В современной литературе достаточно широко обсуждаются вопросы фармакокинетики и фармакодинамики этих лекарственных средств [1, 3, 4]. В то же время скорость всасывания препаратов зависит от целого ряда технических особенностей, к числу которых относятся глубина введения иглы (внутрикожно, подкожно, внутримышечно), выраженность кровотока и наличие липодистрофий в местах инъекций [5-12].
Так, для того чтобы уменьшить вариабельность всасывания инсулина, необходимо осуществлять инъекции в один и тот же анатомический слой тела. Традиционно инсулин вводится в подкожно-жировую клетчатку. Интрадермальные инъекции по скорости попадания инсулина в кровоток сопоставимы с внутривенными инфузиями, но точное попадание в дерму технически очень сложно, так как ее толщина составляет не более 3 мм [13-15]. При внутримышечном введении инсулина короткого действия достигается быстрый эффект, сравнимый с введением аналогов ультракороткого действия, однако отмечается значительная вариабельность всасывания [16]. При внутримышечном введении пролонгированных инсулинов и аналогов инсулина может наблюдаться непредсказуемое действие в виде гипогликемий [17-19]. Кроме этого, осуществление внутримышечных инъекций неприменимо в течение длительного времени из-за болезненности.
Соблюдение ряда правил позволяет минимизировать вариабельность всасывания лекарственных средств и является необходимым условием для достижения их оптимального терапевтического эффекта [20, 21]. Вместе с тем имеющиеся данные свидетельствуют о том, что значительная часть пациентов, получающих инъекционную антигипергликемическую терапию, допускает существенные ошибки, снижающие клиническую эффективность получаемого ими лечения.
Для оценки осведомленности пациентов в технических вопросах инсулинотерапии и определения наиболее часто встречающихся ошибок при проведении инъекций инсулина был разработан специальный опросник, впервые представленный на международном симпозиуме по технике инъекций, проходившем в июне 1997 г. в Страсбурге [22]. Впоследствии опросник был валидирован и использован при проведении анкетирования в 1999–2000 гг. в 7 европейских странах [1, 23, 24].
Спустя несколько лет возникла необходимость в проведении нового исследования по оценке правильности использования инъекционных антигипергликемических препаратов. С сентября 2008 по июнь 2009 г. было проведено международное исследование, охватившее более 43 000 больных СД 1 и 2 типов из 171 центра на территории 16 стран, в том числе из России. Такое количество участников сделало данный опрос самым большим многоцентровым исследованием подобного типа у больных СД. Впервые результаты были представлены на третьем съезде группы экспертов по технике инъекций (Third Injection Technique workshop in AtheNs (TITAN)), проходившем в сентябре 2009 г.
Материалы и методы исследования
Российская когорта была представлена пациентами из Москвы, Санкт-Петербурга, Волгограда, Екатеринбурга. Выборку составили 200 взрослых пациентов (60 мужчин, 140 женщин) с СД1 (70) и СД2 (130), давших согласие на участие в исследовании. Средний возраст пациентов составил 51,7±15,1 лет, средняя длительность СД – 11,9±9,1 лет. Антигипергликемическая терапия инъекционными препаратами (инсулин, эксенатид) проводилась в течение не менее 6 месяцев, в среднем – 8,4±8,5 лет, уровень HbA1c соответствовал 8,4±1,5%, ИМТ – 28,9±6,2 кг/м2.
Демографические и клинические характеристики пациентов в участвовавших центрах представлены в таблице 1.
Опросник, использовавшийся в ходе исследования, состоял из двух частей. Первая часть, заполнявшаяся самостоятельно пациентом, включала 40 вопросов (основные социо-демографические показатели, характер антигипергликемической терапии, различные аспекты использования и введения лекарственных препаратов, обучение вопросам техники инъекций). Вторая часть опросника (12 вопросов) заполнялась медицинскими специалистами, которые оценивали правильность действий пациентов во время инъекций, проводили физикальный осмотр мест введения лекарственных препаратов и фиксировали результат последнего определения HbA1c.
Результаты исследования
В качестве устройства для инъекций 130 (65%) пациентов использовали полуавтоматические дозаторы – шприц-ручки, 39 (19,5%) – одноразовые шприцы, 31 (15,5%) – применяли одновременно оба вида инъекторов. Структура используемых устройств для инъекций в участвовавших центрах представлена в таблице 2.
Иглы одной длины использовали 136 (68,0%) пациентов; одновременно использовали иглы разной длины – 64 (32,0%). Наиболее широко использовались иглы длиной 8 мм, их применяли 122 (61%) обследованных больных; иглами длиной 12,7 мм пользовались 32 (16%) человека, 10 мм – 31 (15,5%), 12 мм – 28 (14%), 6 мм – 19 (9,5%) и 5 мм – 18 (9,0%) пациентов. 25 (12,5%) пациентов не смогли точно ответить на вопрос о длине используемых ими игл.
Пациенты изученной выборки с разной частотой использовали для введения лекарственных препаратов различные анатомические области. 87 (43,5%) обследованных больных осуществляли инъекции в пределах одной анатомической области: в 62 случаях – в передне-брюшную стенку, 19 – в передне-боковую поверхность бедер, 5 – в плечи, 1 – в ягодицы.
113 (56,5%) пациентов вводили лекарственные препараты в несколько анатомических областей. При этом 82 человека использовали две области (53 – живот и бедра, 18 – живот и плечи, 6 – живот и ягодицы, 5 – бедра и плечи); в 29 случаях инъекции проводились в три области (20 – живот, бедра и плечи, 5 – живот, бедра и ягодицы, 3 – живот, ягодицы и плечи, 1 – бедра, плечи и ягодицы); 2 пациента использовали для инъекций все основные анатомические области.
При описании мест инъекций пациентам было предложено указать примерную площадь участка кожи, в пределах которого они проводились. Согласно ответам, 157 (78,5%) опрошенных больных используют площадь, соответствующую 15 × 10 см, 33 (16,5%) охватывают поверхность площадью 8 × 5 см, а в 10 (5%) случаях область инъекций ограничена минимальной площадью 2 × 3 см.
172 (86%) из обследованных пациентов в ходе инъекции формируют кожную складку. При этом отмечены существенные различия в длительности удержания сформированной кожной складки. Лишь 78 (45,3%) из них удерживают ее до полного введения препарата и извлечения иглы. Значительная же часть больных – 46 (26,7%) – отпускают складку еще до введения препарата.
У 83 (41,5%) пациентов в местах инъекций имелись участки уплотнения, при этом изменения подкожной клетчатки были отмечены преимущественно в области живота – в 54, бедер – в 36, плеч – в 26, ягодиц – в 8 случаях. При этом 42 (50,6% из имевших участки липодистрофий) пациента продолжали осуществлять инъекции в измененные участки, причем 12 из них делали это регулярно, 30 – эпизодически. Выявлены различия в уровне HbA1c у пациентов, использующих для инъекций места уплотнений, и тех, у кого не отмечалось изменений подкожной клетчатки – 9,5 и 8,2% соответственно (р=0,02).
Лишь 32 (16%) пациента указали, что места инъекций осматриваются во время каждого посещения эндокринолога. 119 (59,5%) больных не смогли точно указать, когда наблюдавшие их медицинские специалисты проводили оценку состояния мест инъекций.
Теоретические знания и практические навыки, касающиеся техники подкожных инъекций, опрошенные пациенты получили из различных источников: 106 (53%) были обучены врачами-эндокринологами, 44 (22%) – медицинскими сестрами специализированных отделений стационаров, 16 (8%) – средним медицинским персоналом эндокринологических диспансеров, 9 (4,5%) – участковыми врачами. В 28 (14%) случаях необходимые знания были предоставлены больным во время обучения в «Школе диабета». 19 (9,5%) пациентов были обучены технике инъекций немедицинскими специалистами (родителями или другими пациентами с СД) или почерпнули сведения из литературных источников. По мнению пациентов, во время их обучения вопросы, связанные с техникой инъекций, рассматривались с различной частотой (табл. 3). 76 (38%) пациентов обследованной выборки указали, что нуждаются в получении дополнительных знаний в вопросах осуществления инъекций.
Возможность смешивания разных видов инсулина в одном шприце 60 (30%).
При ответе на вопрос о способах утилизации инъекционного инструментария все опрошенные пациенты указали, что помещают использованные иглы и шприцы в обычные корзины для мусора.
Обсуждение результатов
Полученные в ходе исследования данные позволяют заключить, что значительное число пациентов допускает целый ряд серьезных ошибок, осуществляя инъекции антигипергликемических препаратов. Несоблюдение правил введения лекарственных средств может ассоциироваться с ухудшением показателей углеводного обмена, что подтверждается данными других исследований [8, 20]. Это подчеркивает важность формирования технических навыков у всех пациентов перед инициацией инсулинотерапии. Обучение правильной технике инъекций может осуществляться как при проведении занятий в группах («Школа диабета»), так и при индивидуальной работе с пациентом в стационарных или амбулаторных условиях. Основная задача медицинских работников – научить пациентов (или их родственников) правильно выполнять инъекции и решать многочисленные психологические затруднения, с которыми пациент может столкнуться во время проведения инъекций, особенно в самом начале подобной терапии. Медицинские работники должны иметь представление об анатомическом расположении тканей в области инъекции для того, чтобы помочь пациентам избежать внутримышечных инъекций и убедиться, что последующие инъекции выполняются подкожно, без подтекания / обратного вытекания инсулина или других осложнений. Кроме того, медицинские работники должны знать профили всасывания различных препаратов в кровь из различных тканей.
К числу наиболее часто обсуждаемых с медицинскими специалистами вопросов пациенты обследованной выборки отнесли «возможные места инъекций», «необходимость формирования кожной складки» и «необходимость смены мест инъекций в пределах одной области». Несмотря на это, именно в этих вопросах пациенты допускают серьезные неточности.
Имеются литературные данные, показывающие, что не со всеми пациентами проводятся занятия по технике инъекций, но даже с теми, кто получает подобную информацию от медицинских работников, обсуждаются далеко не все важные аспекты правильного выполнения инъекций [24–26].
В данном исследовании было отмечено, что пациенты выбирают возможные места для инъекций без особой системы. Как правило используется ограниченная область, в большом проценте случаев как самими пациентами, так и осматривавшими их медицинскими работниками были отмечены участки уплотнений, осуществление инъекций в которые может приводить к нарушению всасывания препарата и непредсказуемым колебаниям гликемии.
Кроме этого, в значительном числе случаев пациенты либо не формируют кожную складку, либо формируют ее неправильно, либо отпускают ее преждевременно, до введения препарата. Подобные ошибки могут приводить к внутримышечному попаданию лекарственного средства.
Гораздо меньше внимания при работе с пациентами уделяется вопросам выбора длины иглы. А хорошо известно, что именно этот параметр является одним из главных для предотвращения внутримышечных инъекций. Полученные в исследовании результаты, демонстрирующие предпочтение пациентами более коротких игл, согласуются с литературными данными об их эффективности и безопасности [1, 23]. Выбор длины иглы является индивидуализированным совместным решением пациента и его врача, принимаемым с учетом множества факторов, включая физические, фармакологические и психологические [27, 28]. Ранее рекомендовавшиеся длины игл для подкожных инъекций теперь считаются избыточными для многих взрослых (например, 12,7 мм) и для большинства детей (например, 8 мм); и увеличивающими риск инъекции в мышцу. Более короткие иглы безопаснее и, как правило, их применение менее болезненно. Проведенные исследования подтвердили, что даже у пациентов, страдающих ожирением, короткие иглы (5 и 6 мм) и длинные иглы (8 и 12,7 мм) характеризуются сопоставимыми эффективностью и безопасностью / переносимостью [29, 30]. На сегодняшний день нет данных о значимом вытекании инсулина, усилении болевых ощущений, ухудшении контроля над течением СД, увеличении выраженности липогипертрофии или других осложнений в популяции пациентов, использующих короткие (4, 5 и 6 мм) иглы [29–35]. Последние исследования с иглами длинной 4 мм показали, что они безопасны и эффективны у взрослых пациентов с любой массой тела и что такие осложнения, как боль или вытекание инсулина, одинаковы или даже менее выражены по сравнению с более длинными и большего диаметра иглами.
Наконец, наименее освещаемой в повседневной практике является проблема утилизации использованных игл и шприцев. Никто из пациентов обследованной выборки не предпринимает современных мер по утилизации. Во многих странах с этой целью используются устройства для клипирования, хранения использованных шприцев и игл в специальных контейнерах, которые затем сдаются в медицинские или фармацевтические учреждения.
Выводы
- Значительное число пациентов допускает целый ряд серьезных ошибок, осуществляя инъекции антигипергликемических препаратов.
- Несоблюдение правил введения может ассоциироваться с ухудшением показателей углеводного обмена, в связи с чем вопросы техники инъекций должны находиться в центре внимания любого медицинского работника, участвующего в лечении пациентов с СД.
- К вопросам, требующим обязательного обсуждения, должны быть отнесены: режим выполнения инъекций; выбор и методика применения устройств для инъекций; выбор, уход и самостоятельное обследование мест инъекций; правильная техника выполнения инъекции (включая чередование мест введения, угол наклона и оптимальная длина иглы, необходимость формирования кожных складок); возможные осложнения при нарушении техники инъекций и способы их профилактики; вопросы утилизации использованных шприцев и игл.
Новые международные рекомендации по технике инъекций у больных СД
В связи с вышеизложенным были приняты новые международные рекомендации как результат согласованной работы группы экспертов: врачей, медсестер, инструкторов по обучению и психологов из 27 стран [36, 37]. В мае 2010 г. они были переведены на русский язык [38]. В данном документе приведены новые рекомендации по выполнению инъекций для больных СД, основанные на последних научных достижениях и результатах опубликованных исследований. Новые рекомендации дополняют и расширяют уже имеющиеся рекомендации по методике инъекций пациентам с СД [39, 40], а также освещают важные аспекты, упущенные в предыдущих рекомендациях: аналоги инсулина (быстро- и длительнодействующие), препараты агонистов рецепторов ГПП-1, беременность и безопасные иглы. Кроме того, даны дополнительные рекомендации по вопросам, ранее уже анализировавшимся, но оставшимся недостаточно детализированными и ясными: липогипертрофия, педиатрическая практика, шприц-ручки, утилизация использованных игл и процесс обучения.
Рекомендации построены на принципах доказательной медицины. Для градации степени убедительности рекомендаций использовалась следующая шкала:
A – настоятельно рекомендуется;
B – рекомендуется;
C – нерешенный вопрос.
Для градации научной доказательности использовалась следующая шкала.
- По крайней мере, одно рандомизированное контролируемое исследование.
- По крайней мере, одно нерандомизированное (или неконтролируемое или эпидемиологическое) исследование.
- Согласованное экспертное мнение, основанное на опыте, полученном при наблюдении за большим количеством пациентов.
Таким образом, каждая рекомендация сопровождается как буквой, так и цифрой (например A2). Буква свидетельствует о важности рекомендации в повседневной практике, а цифра будет указывать, насколько обоснованное подтверждение она имеет в медицинской литературе. Кроме того, приводятся ссылки на наиболее важные публикации, имеющие отношение к данной рекомендации. Основные рекомендательные положения для пациентов и медицинских работников, соблюдение которых гарантирует надежную доставку инсулина и других противодиабетических препаратов в подкожное пространство, представлены ниже.
- Длина игл, кожные складки, угол наклона. Были упрощены правила подбора оптимальной для пациента длины иглы (табл. 4). У детей и подростков следует применять иглы длинной 5 или 6 мм. Нет медицинских оснований для применения игл длиннее 6 мм. Иглы длинной 5 и 6 мм могут быть использованы у любых взрослых пациентов, включая пациентов, страдающих ожирением. Нет медицинских оснований для применения у взрослых игл длиннее 8 мм. В тех случаях, когда расстояние между поверхностью кожи и мышцами меньше длины используемой иглы, собирание и приподнимание кожной складки или наклон иглы являются обязательным условием.
- Участки для инъекций. Аналоги инсулина и агонисты рецепторов ГПП-1 можно вводить в любые обычно используемые для инъекций области, так как между ними, по-видимому, нет никаких различий в отношении скорости всасывания препарата. Растворимый человеческий инсулин короткого действия следует вводить в область живота, это повысит скорость его всасывания; НПХ-инсулин следует вводить в область бедер или ягодиц с целью замедления его всасывания и снижения вероятности развития гипогликемии. Необходимо избегать случайного внутримышечного введения длительнодействующих аналогов инсулина, так как в таком случае существует высокий риск выраженной гипогликемии.
- Чередование областей. С самого начала инъекционной терапии пациента необходимо обучить простой схеме чередования областей. Согласно одной из схем с доказанной эффективностью область для инъекций разделяется на четыре квадранта (или половины, когда речь идет о бедрах или ягодицах), при этом каждую неделю используется только один квадрант, а затем следующий с чередованием по часовой стрелке, как это показано на рисунках 1 и 2.
- Липогипертрофия. Пациенты должны регулярно осматривать свои области для инъекций инсулина, при этом их необходимо обучить, как выявлять липогипертрофию. Повторно выполнять инъекции в область липогипертрофии нельзя. В настоящее время наилучшими методами профилактики и лечения липогипертрофии считаются применение очищенных человеческих инсулинов или аналогов, регулярное чередование областей для инъекций, использование для инъекций более обширных зон и отказ от повторного использования игл.
- Недопустимость многократного использования одноразовых игл и шприцев. Иглы для шприц-ручек и шприцы следует использовать только один раз. Следует объяснить пациенту возможные последствия, связанные с многократным использованием игл: а) нарушение точности дозирования инсулина вследствие вытекания инсулина или блокировки кристаллами инсулина просвета иглы; б) увеличение риска развития липодистрофий в местах инъекций; в) увеличение риска развития инфекций в местах инъекций; г) появление или усиление болезненных ощущений в месте инъекций.
- Начало инъекционной терапии у детей. Для маленьких детей лучшей методикой будет их отвлечение (до тех пор, пока они не поймут обман) или игра (например, инъекции в мягкую игрушку), а дети постарше лучше реагируют на когнитивно-поведенческую терапию.
- Инъекции подросткам. Подростков следует заверить, что никто не управляет СД идеально все время, а случайные оплошности, если они не становятся привычными, не ведут к неблагоприятному исходу.
- Инъекции взрослым пациентам с СД2. Медицинские работники должны каждого пациента с впервые выявленным СД2 морально готовить к возможному появлению в будущем необходимости использовать инсулин, объяснив ему природу, прогрессирующий характер заболевания, отметив, что варианты лечения включают в том числе инсулинотерапию, и пояснив, что применение инсулина не является признаком неблагоприятного исхода. Настрой на инсулинотерапию должен быть позитивным.
- Инъекции беременным. Страдающая СД (любого типа) беременная женщина, которая продолжает выполнять инъекции в области живота, должна каждую инъекцию осуществлять в собранную кожную складку. На последнем триместре не следует выполнять инъекции в околопупочную область. Можно продолжать выполнять инъекции в боковые стороны живота при условии формирования приподнятой кожной складки.
- Утилизация инъекционного инструментария. Использованные иглы следует собирать в следующем виде (в порядке предпочтения): а) в контейнере, специально разработанном для использованных игл/шприцев; б) если такового нет, то в любом другом проколостойком контейнере, например пластиковой бутылке. Использованные иглы в таких контейнерах следует передавать (в порядке предпочтения): а) в медицинское учреждение (например, больницу); б) другим поставщикам медицинских услуг (например, в лабораторию, аптеку, кабинет врача). Там, где это возможно, следует использовать прибор для клипирования (обламывания) игл. Ни при каких условиях острые предметы нельзя выкидывать в обычные (публичные) урны или мусоросборники. Все заинтересованные лица (пациенты, медицинские работники, фармацевты, должностные лица и производители) несут ответственность (как профессиональную, так и материальную) за достоверно безопасную утилизацию острых предметов.
Благодарность
Выражаем благодарность российскому представительству компании «Бектон Дикинсон» за помощь в проведении анкетирования российской когорты больных и издание на русском языке «Новых рекомендаций по технике инъекций у больных СД».
1. Partanen T.M., Rissanen A. Insulin injection practices // Pract. Diab. Int. — 2000. — 17. — Р. 252-254.
2. Baron A.D., Kim D., Weyer C. Novel peptides under development for the treatment of type 1 and type 2 diabetes mellitus // Curr. Drug. Targets. Immune. Endocr. Metabol. Disord. — 2002. — 2. — Р. 63-82.
3. Hildebrandt P. Subcutaneous absorption of insulin in insulin-dependent diabetic patients. Influences of species, physico-chemical properties of insulin and physiological factors // Danish. Medical. Bulletin. — 1991. — 38. — Р. 337-346.
4. American Diabetes Association Position Statements: Insulin Administration // Diabetes Care. — 2004. — 27. — S106-S107.
5. Vaag A., Damgaard Pedersen K., Lauritzen M., Hildebrandt P., Beck-Nielsen H. Intramuscular versus subcutaneous injection of unmodified insulin; consequences for blood glucose control in patients with type 1 diabetes mellitus // Diabetic. Medicine. — 1990. — 7. — Р. 335-342.
6. Hildebrandt P. Subcutaneous absorption of insulin in insulin-dependent diabetic patients. Influences of species, physico-chemical properties of insulin and physiological factors // Danish. Medical. Bulletin. — 1991. — 38. — Р. 337-346.
7. Frid A Linde B. Clinically important differences in insulin absorption from the abdomen in IDDM // Diabetes Research and Clinical Practice. — 1993. — 21. — Р. 137-141.
8. Johansson U., Amsberg S., Hannerz L., Wredling R., Adamson U., Arnqvist H.J., Lins P. Impaired Absorption of insulin Aspart from Lipohypertrophic Injection Sites // Diabetes Care. — 2005. — 28. — Р. 2025-2027.
9. Thow J.C., Coulthard A., Home P.D. Insulin injection site tissue depths and localization of a simulated insulin bolus using a novel air contrast ultrasonographic technique in insulin treated diabetic subjects // Diabetic Medicine. — 1992. — 9. — Р. 915-920.
10. Thow J.C., Home P.D. Insulin injection technique: depth of injection is important // BMJ. — 1990. — 301. — Р. 3-4.
11. Hildebrandt P. Skinfold thickness, local subcutaneous blood flow and insulin absorption in diabetic patients // Acta. Physiol. Scand. — 1991. — 603. — Р. 41-45.
12. Vora J.P., Peters J.R., Burch A., Owens D.R. Relationship between Absorption of Radiolabeled Soluble Insulin Subcutaneous Blood Flow, and Anthropometry // Diabetes Care. — 1992. — 15. — Р. 1484-1493.
13. Lasagni C., Seidenari S. Echographic assessment of age-dependent variations of skin thickness // Skin Research and Technology. — 1995. — 1. — Р. 81-85.
14. Huzaira M., Rius F., Rajadhyaksha M., Anderson R.R., Gonzбlez S. Topographic Variations in Normal Skin, as Viewed by In Vivo Reflectance Confocal Microscopy // Journal of Investigative Dermatology. — 2001. — 116. — Р. 846-852.
15. Tan C.Y., Statham B., Marks R., Payne P.A. Skin thickness measured by pulsed ultrasound: its reproducibility, validation and variability // Br. J. Dermatol. — 1982. — 106. — Р. 657-667.
16. Frid A., Gunnarsson R., Gьntner P., Linde B. Effects of accidental intramuscular injection on insulin absorption in IDDM // Diabetes Care. — 1988. — 11. — Р. 41-45.
17. Karges B., Boehm B.O., Karges W. Early hypoglycaemia after accidental intramuscular injection of insulin glargine // Diabetic Medicine. — 2005. — 22. — Р. 1444-1445.
18. Frid A., Цstman J., Linde B. Hypoglycemia risk during exercise after intramuscular injection of insulin in thigh in IDDM // Diabetes Care. — 1990. — 13. — Р. 473-477.
19. Vaag A., Handberg A., Laritzen M. et al. Variation in absorption of NPH insulin due to intramuscular injection // Diabetes Care. — 1990. — 13. — Р. 74-76.
20. De Meijer P.H.E.M., Lutterman J.A., van Lier H.J.J., van«t Laar A. The variability of the absorption of subcutaneously injected insulin; effect of injection technique and relation with brittleness // Diabetic Medicine. — 1990. — 7. — Р. 499-505.
21. Strauss K. Insulin injection techniques // Practical Diabetes International. — 1998. — 15. — Р. 181-184.
22. Strauss K. Insulin injection techniques: Report from the 1st International Insulin Injection Technique Workshop, Strasburg, France — June 1997 // Practical Diabetes International. — 1998. — 15. — Р. 16-20.
23. Strauss K., De Gols H., Letondeur C., Matyjaszczyk M., Frid A. The second injection technique event (SITE), May 2000, Barcelona, Spain // Practical Diabetes International. — 2002. — 19. — Р. 17-21.
24. Strauss K., De Gols H., Hannet I., Partanen T.M., Frid A. «A pan-European epidemiologic study of insulin injection technique in patients with diabetes» // Practical Diabetes International 2002; 19: Р. 71-76.
25. Martinez L., Consoli S.M., Monnier L., Simon D., Wong O., Yomtov B., Guйron B., Benmedjahed K., Guillemin I., Arnould B. Studying the Hurdles of Insulin Prescription (SHIP): development, scoring and initial validation of a new self-administered questionnaire // Health Qual Life Outcomes. — 2007. — 5. — Р. 53.
26. Cefalu W.T., Mathieu C., Davidson J., Freemantle N., Gough S., Canovatchel W., OPTIMIZE Coalition. Patients’ perceptions of subcutaneous insulin in the OPTIMIZE study: a multicenter follow-up study // Diabetes Technol. Ther. — 2008. — 10. — Р. 25-38.
27. Becker D. Individualized insulin therapy in children and adolescents with type 1 diabetes // Acta Paediatr Suppi. — 1998. — 425. — Р. 20-24.
28. Uzun S., lnanc N., Azal S. Determining optimal needle length for subcutaneous insulin injection // Journal of Diabetes Nursing. — 2001. — 5. — Р. 83-87.
29. Kreugel G., Keers J.C., Jongbloed A., Verweij-Gjaltema A.H., Wolffenbuttel B.H.R. The influence of needle length on glycemic control and patient preference in obese diabetic patients // Diabetes. — 2009. — 58. — A117.
30. Schwartz S., Hassman D., Shelmet J., Sievers R., Weinstein R., Liang J., Lyness W. A multicenter, open-label, randomized, two-period crossover trial comparing glycemic control, satisfaction, and preference achieved with a 31 gauge x 6 mm needle versus a 29 gauge x 12.7 mm needle in obese patients with diabetes mellitus // Clin. Ther. — 2004. — 26. — Р. 1663-1678.
31. Birkebaek N., Solvig J., Hansen B., Jorgensen C., Smedegaard J., Christiansen J. A 4mm needle reduces the risk of intramuscular injections without increasing backflow to skin surface in lean diabetic children and adults // Diabetes Care. — 2008. — 22. — e65.
32. Jamal R., Ross S.A., Parkes J.L., Pardo S., Ginsberg B.H. Role of injection technique in use of insulin pens: prospective evaluation of a 31-gauge, 8mm insulin pen needle // Endocr. Pract. — 1999. — 5. — Р. 245-250.
33. Kreugel G., Beijer H.J.M., Kerstens M.N., ter Maaten J.C., Sluiter W.J., Boot B.S. Influence of needle size for SC insulin administration on metabolic control and patient acceptance // European Diabetes Nursing. — 2007. — 4. — Р. 1-5.
34. Van Doorn L.G., Alberda A., Lytzen L. Insulin leakage and pain perception with NovoFine 6 mm and NovoFine 12 mm needle lengths in patients with type 1 or type 2 diabetes // Diabetic Medicine. — 1998. — 1. — S50.
35. Clauson P.G., Linden B. Absorption of rapid-acting insulin in obese and nonobese NIIDM patients // Diabetes Care. — 1995. — 18. — Р. 986- 991.
36. Frid A., Hirsch L., Gaspar R., Hicks D., Kreugel G., Liersch J., Letondeur C., Sauvanet J.P., Tubiana-Rufi N., Strauss K. New injection recommendations for patients with diabetes // Diabetes and Metabolism. — 2010. — 36. — s3-s18.
37. Frid A., Hirsch L., Gaspar R., Hicks D., Kreugel G., Liersch J., Letondeur C., Sauvanet J.P., Tubiana-Rufi N., Strauss K. The Third Injection Technique Workshop In Athens (TITAN) // Diabetes and Metabolism. — 2010. — 36. — s19-s29.
38. Frid A., Hirsch L., Gaspar R., Hicks D., Kreugel G., Liersch J., Letondeur C., Sauvanet J.P., Tubiana-Rufi N., Strauss K. Новые рекомендации по тех- нике инъекций у больных сахарным диабетом. — М., 2010. — С?
39. Danish Nurses Organization. Evidence-based Clinical Guidelines for Injection of Insulin for Adults with Diabetes Mellitus, 2nd edition, December 2006. Available from: www.dsr.dk.
40. Association for Diabetescare Professionals (EADV). Guideline: The Administration of Insulin with the Insulin Pen. September 2008. Available from: www.eadv.nl.
Актуальность исследования. Сахарный диабет (СД) – глобальное неинфекционное заболевание, принявшее в XXI веке пандемические темпы распространения. Численность больных СД увеличивается со скоростью, опережающей прогнозы экспертов Всемирной диабетической федерации. За последние 10 лет количество больных увеличилось вдвое и составляет 420 млн человек. Согласно последним прогнозам IDF, к 2040 году ожидается увеличение численности больных до 642 млн человек [1, 2]. Достижение и длительное поддержание компенсации углеводного обмена является основной целью терапевтической тактики при сахарном диабете. Последнее десятилетие ознаменовано неуклонным ростом во всем мире числа пациентов с СД, получающих инсулинотерапию [3]. Инсулинотерапия используется у всех пациентов с СД 1 типа. В последние годы значительно расширились показания к проведению инсулинотерапии у больных с СД 2 типа. По данным Британского проспективного исследования диабета (UKPDS), ежегодно 5–10% больных со впервые диагностированным СД 2 типа требуется терапия инсулином, а спустя 10–12 лет — уже около 80% пациентов нуждаются в постоянной инсулинотерапии [4]. Правильная техника инъекций инсулина является необходимым условием для достижения хорошего контроля СД, снижения вариабельности всасывания и получения оптимального эффекта от использования препарата [5]. В современной литературе достаточно широко обсуждаются вопросы фармакокинетики и фармакодинамики инсулинов. В то же время скорость всасывания препаратов зависит от целого ряда технических особенностей, к числу которых относятся глубина введения иглы, выраженность кровотока и наличие липодистрофии в местах инъекций [1, 3]. Соблюдение ряда правил позволяет минимизировать вариабельность всасывания лекарственных средств и является необходимым условием для достижения их оптимального терапевтического эффекта. Для повышения эффективности инсулинотерапии и улучшения результатов лечения пациентов с СД созданы Российские национальные рекомендации по технике инъекций и инфузий при лечении сахарного диабета 2017 г, в основу которых легли международные рекомендации экспертов, опубликованные в 2015 году. Вместе с тем, значительная часть пациентов, получающих инсулинотерапию, допускает целый ряд серьезных ошибок, которые могут приводить к декомпенсации сахарного диабета и формированию сосудистых осложнений.
Цель. Оценить технические аспекты проведения инсулинотерапии у пациентов с сахарным диабетом 1 и 2 типа.
Задачи исследования. Изучение информированности больных о технике инъекций инсулина и выявление наиболее часто встречающихся ошибок.
Материалы и методы. В исследовании добровольно приняли участие 74 пациента (30 мужчин и 44 женщины) в возрасте от 20 до 76 лет, находящихся на обследовании и лечении в эндокринологическом отделении ГУЗ «Саратовская городская клиническая больница №9». Среди опрошенных было 25 (34%) пациентов с СД 1 типа и 49 (66%) с СД 2 типа. Средняя длительность СД 14,2+9,7 лет. Инсулинотерапия проводилась не менее 6 месяцев, в среднем 9,8+8,6 лет. У большинства пациентов углеводный обмена был декомпенсирован (уровень гликированного гемоглобина составил 8,7+1,7%). Для оценки осведомленности пациентов в технических вопросах инсулинотерапии и определения наиболее часто встречающихся ошибок при проведении инъекций инсулина используется специальный опросник, впервые представленный на международном симпозиуме по технике инъекций, проходившем в июне 1997 г. в Страсбурге [6]. Впоследствии он был неоднократно использован при проведении анкетирования. На основе данного опросника нами составлена анкета, состоящая из 38 вопросов, направленных на оценку основных социодемографических параметров, особенностей применения различных устройств для инъекций, а также выявление наиболее часто допускаемых пациентами ошибок.
Результаты и обсуждение: В качестве устройств для инъекций большинство пациентов (72%) использовали полуавтоматические дозаторы – шприц-ручки, 28% – одноразовые шприцы. Опрошенные пациенты чаще использовали для шприц-ручек иглы длиной 8 мм, их применяли 19 (36 %) и 10 мм 14 (26%) пациентов. Иглы длиной 4 и 5 мм использовались нашими пациентами крайне редко. При этом имеются данные, которые подтверждают эффективность игл меньшей длины (4 мм). Они безопасны и эффективны у взрослых пациентов с любой массой тела и такие осложнения, как боль или вытекание инсулина, одинаковы или даже менее выражены по сравнению с более длинными и большего диаметра иглами [7]. Важное значение имеет использование иглы для шприц-ручки и одноразового шприца только один раз. Повторное использование игл, в частности, связано с развитием липодистрофий [8]. Опрошенные пациенты в среднем за сутки осуществляют 3-4 инъекции инсулина. При таком количестве инъекций, 20 пациентов осуществляют смену игл 1 раз в 3 дня, 21 – 1 раз в неделю, 9 – 1 раз в 2 недели, что крайне не допустимо, а так же в 3-х случаях иглы менялись 1 раз в месяц. Такая же ситуация с использованием одноразовых шприцев, которые 9 пациентов меняли через 3 дня и 9 – через неделю, и всего лишь 1 пациент менял шприц после каждой инъекции. Возможными последствиями, связанными с многократным использованием игл, являются: нарушение точности дозирования инсулина вследствие вытекания инсулина или блокировки кристаллами инсулина просвета иглы; увеличение риска развития липодистрофий и инфекции в местах инъекций; появление болезненных ощущений в месте инъекций. Основными причинами, по которым больные используют иглы повторно, являются удобство и сокращение затрат на расходные материалы. Существует и другое мнение, что использование игл для шприц-ручек повторно менее пяти раз не ведет к прогрессирующей деформации кончика иглы, и, как правило, не связано с развитием липодистрофий, а также не приводит к повышению гликированного гемоглобина и развития инфекций в местах инъекций. Повторное использование иглы – менее влиятельный фактор, чем неправильная ротация мест инъекций или небольшие участки инъекций. Кроме того, повторное использование игл может привести к существенной финансовой экономии в системе здравоохранения [9]. Большинство опрошенных нами пациентов меняют иглы реже, чем предлагают и эти авторы. Ряд исследований показал, что лучший способ сохранить здоровую подкожную клетчатку – это последовательно и правильно чередовать места инъекций инсулина. Нами в ходе опроса было выявлено, что пациенты выбирают возможные места для инъекций без особой системы. Большинство обследованных больных осуществляли инъекции в пределах одной или двух анатомических областей и только 6 пациентов использовали для инъекций все основные анатомические области. Важным аспектом профилактики образования липодистрофии, участков уплотнения является обучение пациентов и применение ими схемы чередования мест инъекций. При опросе выяснилось, что лишь половина опрошенных пациентов знают и применяют схему чередования мест инъекций. Важное значение имеет глубина инъекции инсулина, для этого необходимо правильно формировать кожную складку. В значительном числе случаев пациенты либо не формируют кожную складку, либо формируют ее неправильно, либо отпускают ее преждевременно, до введения препарата. Подобные ошибки могут приводить к внутримышечному попаданию лекарственного средства. Внутримышечные инъекции, особенно в работающую мышцу, могут изменять скорость всасывания и, таким образом, уменьшать максимальные уровни глюкозы в крови во время пиковой активности инсулина и приводить к частой и необъяснимой гипогликемии [10]. При опросе мы выявили, что в значительном числе случаев пациенты либо не формируют кожную складку, либо формируют ее неправильно, либо отпускают ее преждевременно, до введения препарата. Подобные ошибки могут приводить к внутримышечному попаданию лекарственного средства. Большинство наших пациентов не учитывают угол наклона иглы, что также влияет на глубину введения инсулина и, следовательно, на его эффективность. У 12 (16%) опрошенных пациентов имелись участки липодистрофий, при этом 3 пациента продолжали осуществлять инъекции в измененные участки регулярно, 9 – эпизодически, что может приводить к нарушению всасывания препарата и непредсказуемым колебаниям гликемии. Средний уровень гликированного гемоглобина у этих пациентов 9,8+1,9%, а в группе без липодистрофий – 7,9+1,2%. Важная роль отводится медицинскими работниками в обучении пациентов технике инъекций инсулина и осуществлении контроля за правильностью их осуществления. В ходе опроса выявлено, что недостаточно осуществляется контроль за выполнением правил инъекций инсулина, лишь треть пациентов указали, что места инъекций осматриваются во время каждого посещения эндокринолога. Большинство наших пациентов отметили, что теоретические знания и практические навыки, касающиеся техники подкожных инъекций, они получили от врачей-эндокринологов, четверо пациентов были обучены средним медицинским персоналом эндокринологического отделения. Десять больных получили необходимые знания по технике инъекций во время обучения в Школе больных сахарным диабетом. 28 человек отметили несколько источников получения информации, что включало в разных вариациях: школа диабета, врачи-эндокринологи, СМП, интернет источники или литература. Необходимо шире использовать возможность обучения в Школе больных сахарным диабетом для приобретения навыков по технике инъекций инсулина, включая чередование мест введения, угол наклона и выбор оптимальной длины иглы, необходимость формирования кожных складок.
Выводы:
- Пациенты с сахарным диабетом недостаточно информированы о технике инъекций инсулина и допускают целый ряд серьезных ошибок, которые могут приводить к ухудшению углеводного обмена.
- Правильная техника введения инсулина крайне важна для оптимального контроля сахарного диабета, в связи с чем, вопросы техники инъекций должны находиться под контролем медицинских работников.
- При обучении пациентов в Школе больных сахарным диабетом необходимо обращать особое внимание на соблюдение техники выполнения инъекции, возможные осложнения при нарушении техники инъекций и способы их профилактики.