Тест с ответами по теме «Сестринские ошибки лекарственной помощи»
Вашему вниманию представляется Тест с ответами по теме «Сестринские ошибки лекарственной помощи» в рамках программы НМО: непрерывного медицинского образования для медицинских работников (врачи, медсестры и фармацевты).
Тест с ответами по теме «Сестринские ошибки лекарственной помощи» в рамках программы НМО: непрерывного медицинского образования для медицинского персонала высшего и среднего звена (врачи, медицинские сестры и фармацевтические работники) позволяет успешнее подготовиться к итоговой аттестации и/или понять данную тему.
1. Анальгин — частая причина анафилактического шока. Назовите международное непатентованное наименование анальгина
1) амидопирин;
2) баралгин;
3) баралгин М;
4) метамизол;+
5) парацетомол.
2. Больному назначены два препарата для закапывания в глаза. Какое минимальное время должно пройти между закапыванием первого и второго препарата?
1) 1 час;
2) 15 минут;
3) 3-5 минут;+
4) 30 минут;
5) можно закапывать сразу.
3. Важные меры, которые должна предпринять медсестра, чтобы снизить угрозу осложнений лекарственной терапии
1) спросить у пациента, какие препараты ему нельзя применять ни при каких условиях;+
2) проблема осложнений находится в компетенции врача, а не медсестры;
3) уточнить возможные противопоказания;+
4) изучить инструкцию к препарату;+
5) наблюдать за больным после введения препарата.+
4. Врач назначил внутримышечные инъекции Цефтриаксона и велел разводить его 1% раствором Лидокаина. Пациент купил в аптеке Лидокаин -Буфус 100мг/мл. Как можно использовать этот препарат?
1) Лидокаин-Буфус 100 мг/мл — это 0,1% раствор Лидокаина, он непригоден для использования в качестве растворителя;
2) Лидокаин-Буфус 100 мг/мл — это 1% раствор Лидокаина. Его можно использовать для разведения Цефртиаксона;
3) Лидокаин-Буфус 100 мг/мл — это 10% раствор Лидокаина. Его надо развести в 10 раз, чтобы получить назначенную врачом концентрацию растворителя;+
4) Лидокаин-Буфус 100 мг/мл — это 5% раствор Лидокаина, он может быть использован при разведении в 2,5 раза;
5) Лидокаин-Буфус 100 мг/мл можно использовать в качестве растворителя.
5. Врач назначил ребенку лекарство в дозе 50 капель 3 раза в день. Родители не купили пипетку и хотят использовать чайную ложку объемом 5 мл. Сколько ложек препарата следует давать ребенку на один прием?
1) 0,5 чайной ложки;+
2) 1 чайную ложку;
3) 1,5 чайные ложки;
4) 2 чайные ложки;
5) 2,5 чайные ложки.
6. Выберите правильное обращение к пациенту при его идентификации
1) Ваше фамилия «Иванов»?
2) Ваше фамилия «Иванов»? Сергей Степанович?
3) Вы Сергей Степанович?
4) Вы пациент из палаты №15?
5) Назовите, пожалуйста, вашу фамилию имя и отчество.+
7. Выберите правильно заданный вопрос к пациенту при его идентификации
1) Назовите, пожалуйста, вашу фамилию и имя/отчество;+
2) Ваше фамилия Иванов, Сергей Степанович;
3) Вы Сергей Степанович;
4) Вы пациент из палаты №15;
5) Ваша фамилия Иванов.
8. Идентификация пациента — это
1) первичное знакомство медсестры с пациентом;
2) проверка присутствия пациента в отделении;
3) просьба назвать свое имя, чтобы затем вежливо обращаться к пациенту в ходе медицинской процедуры;
4) установление личности пациента и ее соответствия медицинским документам, которое осуществляется перед любой медицинской процедурой;+
5) установление номера истории болезни пациента.
9. Как часто следует менять инфузионную систему у больного, получающего постоянную инфузионную терапию?
1) каждую смену;
2) каждые 12 часов;
3) каждые 24 часа;+
4) каждые 8 часов;
5) после того, как система опустеет.
10. Какие из перечисленных идентификационных признаков нельзя использовать при идентификации больных?
1) адрес;
2) год рождения;
3) номер палаты и номер койки;+
4) фамилию и адрес;
5) фамилию и имя отчество.
11. Какие из перечисленных идентификационных признаков нельзя использовать при идентификации пациента перед проведением медицинского вмешательства?
1) фамилию и имя/отчество;
2) адрес;
3) номер палаты и номер койки;+
4) год рождения;
5) фамилию и адрес.
12. Какой из перечисленных вопросов называют закрытым?
1) Когда у вас возникли боли?
2) От чего у вас усиливаются боли?
3) У вас болит спина?+
4) Что вам помогает от болей в спине?
5) Что у вас болит?
13. Какой из перечисленных вопросов называют открытым?
1) Боли возникают после физической нагрузки?
2) Боли облегчаются после отдыха?
3) Вам помогает анальгин?
4) У вас болит спина?
5) Что у вас болит?+
14. Какой из перечисленных вопросов является закрытым?
1) От чего у вас усиливаются боли;
2) Что у вас болит;
3) Когда у вас возникли боли;
4) Что вам помогает от болей в спине;
5) У вас болит спина.+
15. Какой из перечисленных вопросов является открытым?
1) Что у вас болит;+
2) Вам помогает анальгин;
3) Боли облегчаются после отдыха;
4) У вас болит спина;
5) Боли возникают после физической нагрузки.
16. Какой из перечисленных ниже препаратов не относится к группе препаратов, опасных при ошибочном применении?
1) 10% раствор хлорида натрия;
2) 10% хлористого калия;
3) 40% раствор глюкозы;
4) инсулин;
5) физиологический раствор.+
17. Какой из перечисленных ниже препаратов относят к группе опасных при ошибочном применении?
1) 40% раствор глюкозы;+
2) 5% раствор глюкозы;
3) гемодез;
4) реополиглюкин;
5) физиологический раствор.
18. Какой из перечисленных ниже препаратов считают особенно опасным при ошибочном применении?
1) физиологический раствор;
2) 5% раствор глюкозы;
3) 40% раствор глюкозы;+
4) реополиглюкин;
5) гемодез.
19. Какой микроорганизм является причиной псевдомембранозного колита у пациентов, принимающих макролиды?
1) дизентерийная палочка;
2) клебсиелла;
3) клостридиум дифициле;+
4) стафилококк;
5) энтеровирус.
20. Какой примерный объем капельницы понадобится, если врач хочет, чтобы она простояла всю ночь (8 часов), а скорость введения составляла 20 капель в минуту?
1) 1000 мл;
2) 2000 мл;
3) 400 мл;
4) 500 мл;+
5) 700 мл.
21. Какой примерный объем капельницы понадобится, если врач хочет чтобы она простояла сутки, а скорость введения составляла 20 капель в минуту?
1) 700 мл;
2) 2000 мл;
3) 450-500 мл;
4) 1400 -1500 мл;+
5) 400 мл.
22. Маркировка — это
1) бумажная обертка;
2) запись в истории болезни;
3) запрещающие дорожные знаки;
4) нанесение надписей (условных знаков, букв, цифр, графических знаков) на объект, с целью его дальнейшей идентификации (узнавания), указания его свойств и характеристик;+
5) указатель направления движения.
23. Маркировка инфузионной системы после ее заправки лекарственным препаратом?
1) ФИО больного;
2) ФИО больного, время и дата приготовления, лекарство и растворитель;
3) ФИО больного, время и дата приготовления, лекарство и растворитель, скорость введения;+
4) ФИО больного, лекарство и растворитель, скорость введения;
5) емкость не подписывают.
24. Опасное осложнение эритромицина
1) бессонница;
2) крапивница;
3) псевдомембранозный колит;+
4) пульмонит;
5) стоматит.
25. Основные принципы лекарственной безопасности в сестринской практике:
1) должный способ введения;+
2) контроль влияния медикаментов на состояние пациента;+
3) нужная дозировка;+
4) нужная лекарственная форма;+
5) нужное время;+
6) нужное лекарство;+
7) нужный больной;+

26. Первый уровень контроля при работе с лекарствами гласит:
1) проверяй надпись на ампуле перед тем, как набрать шприц;
2) проверяй надпись на шприце (флаконе) перед введением препарата больному;
3) проверяй надпись на шприце (флаконе) после введения препарата больному;
4) проверяй надпись на этикетке упаковки, когда берешь ее из шкафчика с лекарствами;+
5) проверяй надпись на этикетке упаковки, когда берешь ее, чтобы достать ампулу.
27. Почему 10% хлористого натрия относят к опасным при ошибочном применении?
1) внутривенное введение гипертонических растворов в больших количествах опасно для жизни;+
2) вызывает аллергические реакции;
3) может вызвать остановку сердца;
4) он оказывает раздражающее действие при попадании под кожу;
5) это гипотонический раствор, введение которых опасно для жизни.
28. Почему 10% хлористый кальций относят к препаратам, опасным при неправильном применении?
1) вызывает резкое падение артериального давления;
2) может вызвать тяжелый анафилактический шок;
3) может применяться только под наблюдением врача;
4) попадая в ткани, вызывает их некрозы;+
5) требует проверки на переносимость.
29. Почему 10% хлористого натрия относят к особо опасным при ошибочном применении?
1) внутривенное введение гипертонических растворов в больших количествах опасно для жизни;+
2) он может вызвать остановку сердца;
3) он оказывает раздражающее действие при попадании под кожу;
4) это гипотонический раствор, введение которых опасно для жизни;
5) он вызывает аллергические реакции.
30. Почему запрещено пересыпать (переливать) лекарственные препараты из емкости (упаковки) изготовителя в другую емкость (упаковку)?
1) использование «чужой емкости» запрещено, так как это нарушение санитарно-противоэпидемического режима;
2) использование «чужой емкости» может привести к ошибкам в применении препаратов;+
3) переливание и пересыпание препаратов ведет к нерациональному использованию емкостей и упаковок;
4) переливание и пересыпание препаратов опасно для здоровья медицинского персонала;
5) при переливании и пересыпании препаратов они теряют свое качество.
31. Почему не рекомендовано хранение на одной полке (в соседних ячейках «скоропомощного ящика») 10-миллилитровых ампул сернокислой магнезии и хлористого кальция?
1) это неразумная рекомендация, которая не имеет под собой основания;
2) хлористый кальций – препарат, опасный для пациента при неправильном применении. Ампулы с сернокислой магнезией и хлористым кальцием внешне похожи, совместное хранение может привести к ошибкам при их применении;+
3) у них разная температура хранения;
4) эти препараты имеют разное назначение и должны храниться в разных местах;
5) у них разные режимы хранения.
32. Почему не рекомендовано хранение на одной полке 10-миллилитровых ампул сернокислой магнезии и хлористого кальция?
1) у них разная температура хранения;
2) у них разные режимы хранения;
3) хлористый кальций — препарат, опасный для пациента при неправильном применении. Ампулы с сернокислой магнезией и хлористым кальцием внешне похожи, что может привести к ошибкам при их применении;+
4) эти препараты имеют разное назначение и должны храниться в разных местах;
5) это неразумная рекомендация, которая не имеет под собой основания.
33. Почему при идентификации пациента нельзя задавать закрытие вопросы?
1) закрытые вопросы занимают больше времени;
2) закрытые вопросы могут быть восприняты как оскорбление;
3) закрытые вопросы повышают вероятность ошибки идентификации;+
4) ответы на закрытые вопросы не дают нужной информации;
5) пациенты не любят, когда им задают закрытые вопросы.
34. Почему специалисты по лекарственной безопасности не советуют совместно хранить на одной полке флаконы гепарина и инсулина?
1) у них разная температура хранения;
2) у них разные режимы хранения;
3) флаконы с этими препаратами часто бывают внешне похожими, и это может привести к ошибкам при их применении;+
4) это неразумная рекомендация, которая не имеет под собой основания;
5) это режимные препараты, требующие хранения в разных местах.
35. Правило пяти «П» регулирует вопросы
1) взаимоотношений медсестер и врачей;
2) взаимоотношений с пациентом;
3) лекарственной безопасности;+
4) охраны труда;
5) санитарно-противоэпидемического режима.
36. Правильное суждение о профилактике лекарственных ошибок медицинской сестры
1) чем строже наказание тех, кто совершает ошибку, тем выше безопасность лекарственной помощи;
2) изучение объективных и субъективных причин лекарственных ошибок позволяет сделать вывод: чтобы ошибки не повторялись, необходим системный подход;+
3) нужно создать систему, которая будет работать надежно с учетом средней внимательности персонала и возможных искажениях восприятия;+
4) необходимо быстро выявлять виновников ошибок и строго их наказывать;
5) опытные медсестры, с большим стажем работы, которые смогли довести свои действия до автоматизма, никогда не ошибаются.
37. Правильное суждение об ошибках при проведении инсулинотерапии
1) лекарственные ошибки при введении инсулина не представляют серьезных проблем для здоровья пациентов;+
2) инсулин относят к числу препаратов, при введении которых могут совершаться опасные для пациента ошибки;+
3) жесткий контроль гликемии, стремление держать ее уровень на нормальных цифрах часто ведет к развитию гипогликемии;
4) помимо инсулина, лекарственные ошибки опасные для пациента часто регистрируются при введении катехоламинов, вазопрессоров, препаратов, влияющих на свертываемость крови, седативных средств;+
5) инсулин требует точной дозировки и мониторинга гликемии; даже небольшие нарушения его введения способны причинить существенный вред здоровью пациента.+
38. Препарат, с которого начинают лечение анафилактического шока
1) адреналин;+
2) димедрол;
3) пипольфен;
4) преднизолон;
5) эуфиллин.
39. Препараты, ошибки с которыми особо опасны для жизни и здоровья пациентов
1) прямые антикоагулянты;+
2) морфин;+
3) инсулин;+
4) витамины;
5) антибиотики.
40. При введении этих препаратов могут совершаться опасные для жизни и здоровья пациента ошибки
1) витамины;
2) препараты, влияющие на свертываемость крови;+
3) вазопрессоры (адреналин, норадреналин и др.);+
4) инсулин;+
5) седативные препараты.+
41. Примеры ошибки выбора пути введения лекарственного средства
1) закапывание в глаза новорожденному нестерильных капель;
2) проглатывание таблетки для сублингвального применения;+
3) подключение подачи кислорода в подключичный катетер;+
4) введение энтеральных растворов вместо назогастрального зонда в подключичный катетер;+
5) неправильный расчет дозы химиопрепарата.
42. Принципиальный подход в профилактике ошибок лекарственной терапии основан на
1) правильном ведении документации;
2) правильном подборе руководящих кадров;
3) создании безопасной системы;+
4) на индивидуальной работе с тем, кто совершил ошибку;
5) тщательном поиске и наказании конкретного виновника ошибки.
43. Причины ошибок лекарственной терапии на этапе передачи информации
1) недопонимание, возникшее, когда врач отдает устные распоряжения;+
2) ошибки при переписывании назначений в процедурную тетрадь;+
3) ошибки, связанные с похожим написанием разных лекарственных веществ;+
4) недопонимание, вызванное неразборчивым почерком врача;+
5) сбои в программе компьютера.
44. Рекомендация принять таблетку натощак означает, что пациент должен принять ее
1) когда испытывает голод;
2) на пустой желудок, т.е. за несколько минут до любого приема пищи;
3) утром, после того как выпьет немного жидкости, но до завтрака;
4) перед завтраком;
5) утром, до того как пациент что-либо съест или выпьет.+
45. Системные причины лекарственных ошибок
1) несовершенство организационных процедур фармакологического процесса;+
2) неопределенность в названиях лекарств или их маркировке, инструкциях по применению, медицинских сокращениях или написании;+
3) у ошибок нет системных причин, виноваты конкретные медсестры, которых необходимо наказывать;
4) перегруженность и низкая квалификация медицинских сестер;+
5) несовершенная коммуникация.+
46. Системные причины ошибок, связанных с Лидокаином
1) внешняя схожесть упаковок и ампул с Лидокаином разных концентраций;+
2) безответственность медсестры;
3) широко распространенная «офф-лейбл» практика использования Лидокаина в качестве растворителя для антибиотиков;+
4) безграмотность медсестры, делающей инъекцию;
5) трудности в перерасчетах концентраций растворов.+
47. Системные причины ошибок дозирования инсулина
1) для введения инсулина могут использоваться шприцы с различными шкалами;+
2) инсулиновые шприцы имеют нечеткую шкалу;
3) плохая маркировка флаконов с инсулином;
4) инсулин выпускается в форме различных препаратов, с разным содержанием активного вещества в единице объема и с различной продолжительностью действия;+
5) при использовании инфузоматов, регулирующих скорость введения лекарственных средств, могут допускаться ошибки при настройке скорости.+
48. С какой скоростью следует производить внутривенную капельную инфузию, если врач хочет ввести 100 мл жидкости за 1 час?
1) 100 капель в минуту;
2) 20 капель в минуту;
3) 200 капель в минуту;
4) 30-35 капель в минуту;+
5) 50 капель в минуту.
49. С какой скоростью следует производить внутривенную капельную инфузию, если врач хочет ввести 200 мл жидкости за 1 час?
1) 10 мл, или 200 капель в минуту;
2) 1мл, или 20 капель в минуту;
3) 2 мл, или 40 капель в минуту;
4) 3,3 мл, или 60-70 капель в минуту;+
5) 5 мл, или 100 капель в минуту.
50. С какой скоростью следует производить внутривенную капельную инфузию, если врач хочет ввести 300 мл жидкости за 1 час?
1) 1 мл, или 20 капель в минуту;
2) 10 мл, или 200 капель в минуту;
3) 2 мл, или 40 капель в минуту;
4) 5 мл, 100 капель в минуту;+
5) струйно.
51. С какой скоростью следует производить внутривенную капельную инфузию, если врач хочет ввести 600 мл жидкости за 1 час?
1) 50 капель в минуту;
2) 100 капель в минуту;
3) 10 мл в мин, 200 капель в минуту;+
4) 20 капель в минуту;
5) 30-35 капель в минуту.
52. С какой скоростью следует производить внутривенную капельную инфузию, если врач хочет ввести 60 мл жидкости за 1 час?
1) 50 капель в минуту;
2) 30-35 капель в минуту;
3) 200 капель в минуту;
4) 1 мл в мин, 20 капель в минуту;+
5) 100 капель в минуту.
53. Сколько времени может пройти от момента приготовления лекарственного раствора до его введения пациенту?
1) не более 10 минут;
2) не более 3 часов;
3) не более 30 минут;+
4) не более суток;
5) раствор должен быть введен в течение рабочей смены.
54. Сколько идентификационных признаков используют при идентификации пациента?
1) 1;
2) 2;+
3) 3;
4) 4;
5) 5.
55. Сколько капель содержится в 1 мл водного раствора?
1) 10;
2) 20;+
3) 25;
4) 30;
5) 50.
56. Сколько капель содержится в 10 мл водного раствора?
1) 100;
2) 1000;
3) 200;+
4) 300;
5) 500.
57. Сколько капель содержится в 100 мл водного раствора?
1) 1000;
2) 10000;
3) 2000;+
4) 20000;
5) 500.
58. Сколько мл водного раствора содержится в 100 каплях этого раствора?
1) 100мл;
2) 10мл;
3) 1мл;
4) 50мл;
5) 5мл.+
59. Сколько мл водного раствора содержится в 200 каплях этого раствора?
1) 50 мл;
2) 1 мл;
3) 5 мл;
4) 100 мл;
5) 10 мл.+
60. Сколько мл водного раствора содержится в 40 каплях этого раствора?
1) 100 мл;
2) 2 мл;+
3) 50 мл;
4) 1 мл;
5) 5 мл.
61. Сколько мл водного раствора содержится в 60 каплях этого раствора?
1) 3 мл;+
2) 1 мл;
3) 100 мл;
4) 10 мл;
5) 50 мл.
62. Сколько уровней контроля осуществляет медсестра процедурного кабинета при работе с лекарствами?
1) 1;
2) 2;
3) 3;
4) 4;+
5) 5.
63. У пациентки аллергия на Анальгин. Какой из перечисленных ниже анальгетиков можно назначить этой пациентке, не опасаясь аллергической реакции?
1) парацетамол;+
2) метамизол натрия;
3) баралгин (содержит метамизол и спазмолитик);
4) баралгин М (чистый метамизол);
5) пенталгин, содержащий парацетамол, коффеин и спазмолитик;+
6) пенталгин, содержащий метамизол натрия, коффеин и спазмолитик.
64. У пациентки была аллергическая реакция на анальгин. Какой из перечисленных ниже анальгетиков можно назначить этой пациентке, не опасаясь аллергической реакции?
1) баралгин (содержит метамизол и спазмолитик);
2) баралгин М (чистый метамизол);
3) метамизол;
4) парацетомол;+
5) пенталгин с метамизолом натрия.
65. Формула перевода капель водного раствора в мл?
1) число капель:10;
2) число капель:20;+
3) число капель:25;
4) число капель:30;
5) число капель:50.
66. Цена деления в шприце – это
1) объем шприца;
2) объем жидкости, набираемый в шприц, когда поршень шприца сдвигают на 1 маленькое деление;+
3) объем жидкости, набираемый в шприц, когда поршень шприца сдвигают на 5 маленьких делений;
4) стоимость шприца;
5) объем жидкости, набираемой в шприц, при сдвигании поршня на большое деление, состоящее из 10 маленьких.
67. Цена деления инсулинового шприца для набора инсулина, содержащего 100 ед. в 1 мл
1) 10 мл;
2) 0, 001 мл;
3) 1 мл;
4) 0,1 мл;
5) 0, 01 мл — содержит 1 ед. инсулина.+
68. Частые причины лекарственных ошибок, требующие системных мер по их устранению
1) совместное хранение лекарств, опасных при неправильном применении;++
2) небрежное ведение листов назначений, например, в листе назначения легко перепутать мг и мл;++
3) системных мер снижения риска ошибок не существует, необходимо работать индивидуально с каждым конкретным виновником, совершившем ошибку;
4) невнимание к сбору аллергоанамнеза;
5) ошибки при устной передаче информации.
69. Четвертый уровень контроля при работе с лекарствами гласит:
1) проверяй надпись на ампуле перед тем, как набрать шприц;
2) проверяй надпись на шприце (флаконе) перед введением препарата больному;+
3) проверяй надпись на шприце (флаконе) после введения препарата больному;
4) проверяй надпись на этикетке упаковки, когда берешь ее из шкафчика с лекарствами;
5) проверяй надпись на этикетке упаковки, когда берешь ее, чтобы достать ампулу.
Специальности для предварительного и итогового тестирования:
Общая практика, Операционное дело, Организация сестринского дела, Организация здравоохранения и общественное здоровье, Сестринское дело, Скорая и неотложная помощь, Стоматология, Управление сестринской деятельностью.
Уважаемые пользователи!
Каждый тест проходится вручную.
Это колоссальный труд авторов.
В это непростое время мы делаем все, чтобы сохранить Ваше время. Если хотите сказать Спасибо, то можете просто отправить ДОНАТ.
Спасибо, что Вы с нами!
Врач может назначить Вам одну или две инъекции продленного инсулина в сутки (утром и вечером).
Сколько инъекций (1 или 2) будет назначено, зависит от времени действия конкретного препарата инсулина (действует он сутки или меньше) и от инсулина, который вводится на еду.
Часто днем фон обеспечивается за счет «хвостов» пищевого инсулина, а длинный инсулин вводится только на ночь.
При схеме, при которой дневной фон поддерживается за счет пищевого инсулина, следует помнить, что если Вы будете пропускать прием пищи и не вводить короткий инсулин, то Вам днем не хватит фонового инсулина.
Потребность в базальном инсулине может меняться в течение суток. Но в целом, правильно подобранная доза базального инсулина в обычном режиме (без острых заболеваний и пр.) меняется редко. Не надо без причины каждый день изменять дозу базального инсулина. Регулировать колебания глюкозы крови в результате приема пищи надо коротким инсулином.
Доза базального инсулина адекватна, если глюкоза крови в пределах целевого уровня утром натощак, ночью и в период пропусков пищи.
Базальный ночной инсулин должен «держать» тот уровень глюкозы, который был перед сном. Т.е. если доза базального инсулина подобрана правильно, то с каким сахаром Вы легли спать, с таким и должны встать.
Какие существуют требования к базальным инсулинам?
Основное требование – отсутствие пика действия. Инсулин должен действовать максимально ровно. Иначе на пике действия возможны гипогликемии. Все генно-инженерные базальные инсулины (протамин, хумулин Н, базал, генсулин Н, протафан и др.) являются пиковыми (имеют пик действия) и это их существенный недостаток. Профиль действия этих инсулинов такой: начало — через 1-2 часа с момента подкожного введения; «пик» — 5-8 часов; общая продолжительность действия — 16-18 часов (изначально была заявлена 24 часа).
Аналоги сверхдлительного действия (лантус, гларгин, левемир, туджео, тресиба) являются беспиковыми инсулинами (инсулины «плоского» действия) и это их огромное преимущество.
Как правильно подобрать фоновый инсулин?
При диабете 2 типа часто инсулинотерапия начинается с инъекции инсулина на ночь («подколка»). При диабете 1 типа базальный инсулин также часто вводится 1 раз вечером.
Оценивать дозу вечернего базального инсулина необходимо по уровню глюкозы крови ночью и утром.
Ночью и утром уровень глюкозы крови находится в пределах целевого уровня, значит, доза инсулина подобрана правильно.
Часто на практике увеличение дозы ночного базального инсулина осуществляется по уровню глюкозы натощак. Если глюкоза крови утром выше целевых значений, просто увеличивается доза ночного инсулина. Это не совсем верный подход. Необходимо сначала разобраться, почему утром высокий уровень глюкозы.
Утренняя гипергликемия – одна из самых сложных проблем в лечении сахарного диабета.
Причиной высокого уровня гликемии утром могут быть:
- Высокий уровень гликемии перед сном.
- «Поздний ужин»: («медленная» еда вечером, которая «вылазит» ночью и «висит» всю ночь).
- Недостаток инсулина.
- Недостаточная продолжительность действия инсулина.
- Ночные гипогликемии.
- Феномен «утренней зари».
- «Ранний ужин» при СД 2.
- Рост уровня глюкозы после пробуждения («стресс пробуждения», феномен «ноги на пол»).
В этом перечне не перечислены такие технические причины, как неисправность шприц-ручки, загиб канюли, испорченный инсулин, введение в места липодистрофий и др.
Чтобы проверить дозу базального ночного инсулина, надо правильно поужинать. Ужин должен быть не позднее, чем за 4 часа до сна. Также ужин должен быть необильным и «легким». При проверке базы на ужин нельзя есть макароны, гречку, перловку, сложные продукты (пельмени, блины, плов и пр.), творог и продукты из него (сырники, запеканка и др.), жирные продукты. Можно: пшенную кашу, геркулес, отварную картошку, отварные и свежие овощи, отварное мясо, отварная рыба, хлеб. Смысл раннего ужина: если поужинать поздно и соответственно поздно ввести короткий инсулин, то действие короткого инсулина наслоится на действие базального инсулина и нельзя будет правильно оценить дозу базального инсулина. Смысл «легкого» ужина: продукты должны усвоиться организмом до того, как человек ляжет спать, т.е. еда должна быть «быстрой». Если поужинать «медленной» едой, она «вылезет» ночью и всю ночь будет повышать уровень глюкозы крови.
Следующий момент – замеры глюкозы. Если нет мониторинга, замеры надо делать как минимум 5 раз: перед сном; в 00.00; в 03.00; в 06.00 и перед завтраком. Для этого заводится будильник (или спящему пациенту измеряет другой человек). Еще лучше измерять каждые 2 часа. Желательно (многие считают, что обязательно) такую проверку проводить не одну ночь, а три ночи, что исключить случайные колебания. Если четко вырисовывается проблемный участок, на нем надо провести замеры каждый час.
Какие возможны варианты
1) Глюкоза ночью и утром в пределах целевого уровня – оптимальная доза базального инсулина.
2) Линейный рост — нехватка базального инсулина (мало инсулина).
На мониторинге мы видим, что глюкоза крови с 01.00 непрерывно растет, значит надо увеличивать дозу базального инсулина. Но, если на ужин ели «тяжелую» пищу (пельмени, макароны, много мяса и др.), то это может «вылезать» еда!
3) Рост глюкозы крови начинается ближе к утру и растет постепенно — недостаточная продолжительность действия инсулина (инсулин «не тянет» до утра).
Что можно сделать в таком случае:
а) сместить время инъекции на более позднее время;
б) попробовать увеличить дозу инсулина – если нет тенденции к низкому уровню глюкозы;
в) вводить инсулин в более «медленное» место (ногу);
г) заменить инсулин на аналог.
4) Низкий уровень глюкозы ночью, а утром высокий. Такая ситуация говорит об избытке базального инсулина.
Если доза базального инсулина избыточна, то ночью может быть низкий уровень глюкозы крови, на что организм реагирует выбросом гликогена из печени и уровень глюкозы крови растет (так называемый «откат»). Гипогликемия чаще возникает на пике действия инсулина длительного действия (если вводится «пиковый» инсулин). Гипогликемию человек может и не почувствовать. Может быть просто приступ потливости (человек просыпается весь мокрый), человеку могут сниться кошмары, а также могут возникнуть другие неспецифические симптомы. Гипогликемия может длиться несколько минут и ее можно не «поймать» при измерении глюкозы (иногда даже на мониторинге). Вместо гипогликемии фиксируются высокий уровень глюкозы и увеличивается доза инсулина. Но вместо снижения глюкозы крови получаем еще больший рост. Такая ситуация часто встречается при введении «пиковых» инсулинов. Это синдром Сомоджи — синдром передозировки инсулина.
5) Резкий рост глюкозы под утро — «утренняя заря».
В такой ситуации мы видим, что ночью глюкоза находится в целевом диапазоне, но с 4-5 утра начинается резкий рост. Борьба с «зарей» непроста. Если человек на помпе, на это время выставляется большая доза введения инсулина. Если нет, «зарю» надо «скалывать» коротким инсулином. И часто «скалывать» надо на предупреждение (т.е. путем мониторинга или частых замеров четко определяется, в какое время начинается заря, и короткий инсулин вводится до этого времени, т.к. когда «заря» развернулась, «сколоть» ее непросто).
6) Рост уровня глюкозы после пробуждения («стресс пробуждения», феномен «ноги на пол»).
Ситуация похожа с «утренней зарей», но возникает после того как человек проснулся. Т.е. человек проснулся с нормальным уровнем глюкозы крови, получает базальный инсулин суточного действия, не завтракает и не вводит инсулин короткого действия. Казалось бы, глюкоза крови не должна расти (еды нет, базальный инсулин есть). Однако нередко, чем дольше не ест человек, тем больше растет глюкоза и плохо «скалывается» коротким инсулином. Это печень начинает Вас «кормить», раз не хотите есть сами. В такой ситуации надо ввести привычку завтракать вскоре после пробуждения.
В целом, ситуации с утренней зарей, передозировкой или нехваткой инсулина бывает очень сложно дифференцировать.
Проверка базального инсулина в течение дня осуществляется пропуском пищи. Чтобы оценить базу с утра до обеда, утром не вводится короткий инсулин, до обеда ничего не есть, измерять глюкозу каждый час. Чтобы оценить участок с обеда до ужина, между завтраком и ужином должно пройти не менее 4 часов, в обед не вводится короткий инсулин, пропускается обед, измеряется глюкоза каждый час. Аналогично – участок от ужина до сна. На протяжении всего проверяемого периода не должно быть перекусов, введения дополнительных доз инсулина.
Способ проверки базы пропуском еды не подходит, если дневной фон обеспечивается за счет «хвостов» короткого инсулина (т.е. инсулин длительного действия с продолжительностью действия менее 12 часов вводится 1 раз в сутки на ночь). Проверка базы должна в отсутствие физической активности, острых заболеваний, стрессов. Нельзя проверять базу после перенесенной гипогликемии.
Некоторые технические проблемы инсулинотерапии и пути их решения
Как цитировать:
Никонова Т.В. Некоторые технические проблемы инсулинотерапии и пути их решения. Проблемы эндокринологии.
2012;58(6):60‑64.
Nikonova TV. Certain technical problems of insulin therapy and approaches to their solution. Problemy Endokrinologii. 2012;58(6):60‑64. (In Russ.)

В первые годы инсулинотерапии приходилось сталкиваться с многочисленными техническими трудностями. Дж. Маклеод (сотрудники которого Ф. Бантинг и Ч. Бест в 1921 г. получили инсулин) писал в своей книге «Инсулин и его применение в лечении диабета»: «Чтобы больной мог доверить самому себе свою собственную жизнь, ему нужно отлично овладеть определением дозы и введением инсулина». Это утверждение верно и сегодня, так как единственным методом лечения сахарного диабета 1-го типа (СД1) остается подкожное введение инсулина. Важным является правильное использование и инсулина, и современных средств его введения, к которым относятся шприцы, шприц-ручки и инсулиновые помпы.
Инсулин, как и любой другой лекарственный препарат, имеет ограниченную длительность хранения. На каждом флаконе или картридже указывается срок его годности. Запас инсулина должен храниться в холодильнике при температуре 2—8 °С, используемый препарат должен иметь комнатную температуру. Известно, что инсулин снижает свою активность под действием прямого солнечного света, поэтому после инъекции следует убирать флакон или шприц-ручку в упаковку. Инсулиновые шприцы по-прежнему являются альтернативой шприц-ручкам и позволяют вводить инсулин с высокой степенью дозирования. Особое внимание следует обращать на соответствие инсулина и используемого инсулинового шприца. До сих пор встречаются шприцы для инсулина с концентрацией 40 ЕД/мл, при этом в мире в настоящее время в основном выпускаются инсулины с концентрацией 100 ЕД/мл. Использование шприцев U-40 при наборе инсулина с концентрацией U-100 может приводить к значительным ошибкам в дозировании и тяжелым гипогликемиям. Шприцы желательно использовать один раз.
Первая шприц-ручка (полуавтоматический дозатор инсулина) появилась в 1985 г. Исходно шприц-ручки были разработаны для больных с нарушением зрения, которые не могли самостоятельно набрать инсулин в шприц. В дальнейшем их стали использовать все больные СД, так как они создают для больного определенные удобства, особенно при современных режимах интенсифицированной инсулинотерапии, когда приходится делать инъекции многократно в течение дня. Однако обращение со шприц-ручками в определенном смысле несколько сложнее, так что больные должны тщательно изучить инструкцию по использованию и строго ее придерживаться. Один из недостатков шприц-ручек состоит в том, что, когда в картридже остается небольшое количество инсулина (меньше нужной дозы), многие больные выбрасывают такой картридж и вместе с ним инсулин. Желательно, чтобы шприц-ручки имели шаг набора дозы не больше 1 ЕД, а для детей — даже 0,5 ЕД. Иглы для шприц-ручек должны использоваться только один раз. Чтобы сделать введение инсулина практически безболезненным, острие иглы подвергается специальной заточке и смазке с использованием новейших технологий. При многократном использовании игла затупляется, что может приводить к излишней травматизации подкожной клетчатки и развитию липогипертрофий. Часто больные продолжают вводить инсулин в эти уплотнения, так как инъекции инсулина в них менее болезненны. Однако всасывание инсулина из липодистрофических уплотнений неравномерное, что может ухудшить эффект. В настоящее время шприц-ручки выпускаются практически всеми зарубежными производителями инсулинов, а также производителями медицинского оборудования.
Шприц-ручка Лантус SoloSTAR была представлена в 2007 г., с ее помощью можно одновременно вводить до 80 ЕД инсулина в отличие от других шприц-ручек, которые позволяют ввести не более 60 ЕД. Шприц-ручка предварительно заполнена инсулином и утилизируется, когда кончается инсулин. Таким образом, отпадает необходимость менять картриджи инсулина, что существенно облегчает пользование такой шприц-ручкой. Шприц-ручка SoloSTAR имеет шаг набора в 1 ЕД. и возможность хода вперед/назад, т.е. обладает всеми свойствами современного средства введения инсулина.
Важным практическим аспектом инсулинотерапии с использованием шприц-ручек является усилие, которое необходимо применить для инъекции. В исследовании T. van der Burg и соавт., 2011 [1] сравнивались усилия, необходимые для введения инсулина с помощью шприц-ручки SoloSTAR (SoloSTAR; «Sanofi-Аventis») и других одноразовых шприц-ручек при различной скорости инъекции, рассчитываемой по объему выводимого инсулина. Исследовано 4 разных типа шприц-ручек: SoloSTAR с инсулином гларгин (серийный номер 40U286), FlexPen с инсулином детемир (серийный номер VH70215), NGFP с инсулином детемир (серийный номер VH70007) и KwikPen с инсулином лизпро (серийный номер A477063). Протестировано по 20 шприц-ручек каждого типа при двух скоростях введения инсулина (6 и 10 ЕД/с). Все тесты проводились с иглами, рекомендованными производителями, с одинаковым внешним диаметром 0,25 мм: BD Micro-Fine 0,25 мм (31 G) × 5 мм для SoloSTAR и KwikPen; NovoFine 0,25 мм (31 G) × 6 мм для FlexPen и NGFP. Тестирование проводилось с использованием тензометра («Zwick GmbH & Co. KG», Ульм, Германия) и датчика усилия (KAF-TC, Zwick GmbH & Co. KG, Ульм, Германия; номинальная нагрузка 200 Ньютон – Н) при стандартных атмосферных условиях. Предварительно было показано, что усилие, необходимое для инъекции инсулина, зависит в основном от следующих факторов: трения между движущимися частями механизма, трения между клапаном и стеклянной частью картриджа, трения жидкости (инсулина) и давления тканей. Поскольку давление тканей трудно измерить и воспроизвести в эксперименте с высокой степенью постоянства, во всех тестах инсулин из шприц-ручек выводился в стакан.
Из 4 одноразовых инсулиновых шприц-ручек для SoloSTAR понадобилось самое меньшее усилие независимо от вводимой дозы. При введении большей дозы у всех 4 ручек требовалось большее усилие, однако у SoloSTAR оно было существенно меньше, чем у других шприц-ручек. Эта разница наблюдалась как в отношении среднего, так и максимального усилия. Результаты этого исследования соответствуют опубликованным ранее данным лабораторных исследований, по которым SoloSTAR требовала меньшего усилия для инъекций, чем FlexPen [2]. Вместе с тем результаты исследований J. Rissler и соавт. [3] и T. Asakura и соавт. [4] указывают на меньшее усилие для инъекций у NGFP, чем у SoloSTAR. Несовпадение данных объясняется тем, что в упомянутых исследованиях ориентировались на линейную скорость (в мм/с) без учета объемной скорости (ЕД/с). В связи с различиями механизмов шприц-ручек, объем инсулина, высвобождаемый в секунду, у SoloSTAR на 27,5% больше, чем у FlexPen и NGFP.
В наблюдательном обзорном клиническом исследовании J. Сarter и соавт., 2008 [5] была показана высокая удовлетворенность пациентов шприц-ручками SoloSTAR. В данном исследовании подавляющее число участников отметили легкость обучения использованию и простоту применения. Установлено положительное воздействие на различные психологические аспекты пациентов, в том числе преодоление нежелания использовать инсулин и повышение уверенности в способности управлять своим диабетом даже для пациентов с нарушениями подвижности кистей рук.
В исследовании T. Haak и соавт. [6], в котором нарушения кистевой моторики имелись у 16 пациентов и у 19% пациентов были нарушения зрения, большинство участников сочли SoloSTAR удобнее для инъекций 40 ЕД инсулина по сравнению с FlexPen. Результаты этого исследования могут быть связаны с меньшим усилием, необходимым для инъекций [2]. Следует отметить, что это исследование проводилось в лабораторных условиях, при этом инсулин выводился в стакан, а не в ткань. Поэтому ощущения пациентами усилия в повседневной практике могут отличаться от экспериментальных результатов.
На действие инсулина после подкожной инъекции влияет много факторов, в том числе выбор места инъекции [7, 8], скорость всасывания из подкожной клетчатки [9], тип инсулина, условия окружающей среды. Инъекции должны всегда осуществляться в подкожно-жировую клетчатку, а не внутрикожно или внутримышечно. Попадание инсулина в мышечный слой может привести к непредсказуемым колебаниям гликемии. Для того чтобы избежать внутримышечной инъекции, используются короткие инсулиновые иглы — длиной 4, 5, 6 мм. У взрослых пациентов инъекции с помощью коротких игл не требуют формирования кожной складки; они должны выполняться под прямым углом к поверхности кожи. Для инъекций инсулина используется несколько областей: передняя поверхность живота, бедер, наружная поверхность плеч, ягодицы. Быстрее всего инсулин всасывается из области живота, инсулин короткого действия перед приемом пищи рекомендуется вводить именно в эту область, пролонгированный инсулин можно вводить в бедра или ягодицы.
Важное значение имеет точность дозирования инсулина [10]. В открытом рандомизированном исследовании N. Hermann [11] определялась точность дозирования инсулина с использованием шприц-ручек SoloSTAR с инсулинами гларгин (Лантус) и глулизин (Апидра). Шесть различных доз инсулина (10, 40 и 80 ЕД гларгина и 5, 15 и 30 ЕД глулизина) вводили в губку. Шприц-ручки взвешивали до и после выведения тестируемой дозы. Точность дозирования подсчитывалась согласно рекомендациям международной организации по стандартизации (ISO). Средние стандартные отклонения доз гларгина оставляли 0,24, 0,36 и 0,62 ЕД. для 10, 40 и 80 ЕД соответственно. Средние стандартные отклонения доз глулизина — 0,20, 0,29 и 0,34 ЕД для 5, 15 и 30 ЕД соответственно. Таким образом, исследование показало большую точность дозирования инсулинов в шприц-ручках SoloSTAR в соответствие со стандартами ISO. Высокая точность дозирования инсулина способствует улучшению гликемического контроля.
В отличие от других шприц-ручки SoloSTAR для базального и болюсного инсулинов имеют разный цвет, что позволяет больным легче различать эти инсулины, даже в случае плохого зрения. В исследовании F. Austin [12] было продемонстрировано, что цвета шприц-ручек SoloSTAR легко различить при тусклом свете; даже люди с нарушенным цветовосприятием четко видят отличия. Возможность дифференцировать инсулиновые шприц-ручки сводит к минимуму риск введения «не того» инсулина и соответственно уменьшает риск возникновения побочных эффектов лечения. Шприц-ручки SoloSTAR — единственные шприц-ручки, имеющие различный цвет корпуса, кнопки инъекции и селектора дозы для разных инсулинов.
Компанией «Sanofi» были выпущены также человеческие инсулины Инсуман Рапид и Инсуман Базал в одноразовых шприц-ручках SoloSTAR, которые имеют шаг набора в 1 ЕД, максимальную единовременную дозу инсулина до 80 ЕД, при этом дозу легко установить и адаптировать, хорошо слышны щелчки при наборе, легко подтвердить введение полной дозы (селектор возвращается к «0»), легко дифференцировать шприц-ручки, так как они имеют разные цвета для Инсумана Рапид и Инсумана Базал. В случаях назначения инсулина НПХ или фиксированных инсулиновых смесей, содержащих инсулин НПХ, к факторам, влияющим на действие инсулина, прибавляется еще один — степень гомогенности кристаллической суспензии. Все используемые в настоящее время НПХ-картриджи требуют проведения перед инъекцией тщательного перемешивания кристаллической суспензии, поскольку без надлежащей гомогенизации препарата может наблюдаться значительная вариабельность вводимой дозы. Точное дозирование инсулина НПХ достигается при как минимум 10-кратном переворачивании картриджа или «прокатывании» его в течение определенного времени между ладонями. Во избежание образования пузырьков картридж нельзя встряхивать. Согласно инструкциям по применению инсулина НПХ в картриджах, для получения гомогенной суспензии необходимо переворачивать картридж не менее 10 раз. С другой стороны, в реальной практике считается, что процедура перемешивания суспензии инсулина раздражает пациентов. P. Jehle и соавт. [13] обнаружили, что неадекватное ресуспензирование инсулина НПХ перед инъекцией шприц-ручкой — нередкое явление среди пациентов. Хотя авторы не определяли точную дозу инсулина, они оценивали ее косвенно по оптической плотности суспензии. Мутность суспензии была обусловлена наличием в ней комплексов инсулина, тогда как прозрачность определялась растворителем или растворенным инсулином в зависимости от используемого препарата. Лишь 10 (9%) из 109 больных, участвовавших в исследовании, перемешивали инсулин правильно, переворачивая картридж или прокатывая его между ладонями не менее 10 раз. После того, как пациентов обучили правильной технике ресуспензирования, авторы отметили, что у пациентов, соблюдающих эту технику, частота эпизодов гипогликемии была значимо ниже, чем у несоблюдавших. Авторы рекомендовали переворачивать ручки с инсулином НПХ не менее 20 раз, причем эта рекомендация должна была включаться в программу обучения больных. Позднее было показано, что только один из 180 пациентов перемешивает инсулин в соответствии с инструкцией производителя. В 40% картриджей, наполовину опустошенных пациентами, оптическая плотность суспензии инсулина значительно отличалась от ожидаемой. Таким образом, больные часто пренебрегают правилами перемешивания суспензии инсулина. Современные картриджи инсулина НПХ содержат в растворе специально разработанные шарики, помогающие перемешиванию. Однако этот компонент в настоящее время не стандартизирован, сами шарики значительно варьируют как по количеству (от одного до трех), так и по материалу изготовления (металл, стекло).
P. Kaiser и соавт. [14] оценивали эффективность перемешивания инсулина НПХ с меньшей кратностью переворачиваний, чем рекомендовано. В исследовании использовались картриджи с инсулином НПХ производства «Sanofi-Aventis», «Lilly», «Berlin-Chemie», «B. Braun и Novo Nordisk» (см. таблицу).
С целью имитации ежедневного режима лечения пациента картриджи с инсулином опустошались на 28 МЕ утром и вечером в течение 5 дней. Первую дозу получали после стандартной процедуры ресуспензирования (20 переворачиваний картриджа), последующие дозы получали после 3, 6, 10 или 20 переворачиваний (12 картриджей в каждой экспериментальной серии, две дозы в день). Концентрацию инсулина в дозах 1, 2, 6, и 10 определяли методом жидкостной хроматографии высокого давления. В первых корректно приготовленных дозах наблюдались сравнимые концентрации инсулина.
В большинстве остальных образцов были выявлены явные и значительные отклонения от заданной дозы, особенно при 3- и 6-кратном переворачивании картриджа. Достичь эффективного ресуспензирования путем меньшего числа переворачиваний удалось только в картриджах «Sanofi-Aventis», содержащих три более тяжелых металлических шарика. Во всех остальных картриджах с меньшим количеством шариков при несоблюдении официальной инструкции по применению была велика вероятность получения неправильной дозы. Все применявшиеся в данном исследовании картриджи обеспечивают точное дозирование инсулина при его 20-кратном перемешивании в соответствии с инструкцией производителя. Неадекватность дозирования вследствие низкой гомогенизации при несоблюдении инструкции по применению может приводить к увеличению дозировок инсулина, что должно учитываться при планировании затрат на лечение. Кроме того, введение инсулина с низкой концентрацией действующего вещества может привести к повышению концентрации оставшейся в картридже части суспензии и соответственно увеличению риска превышения концентрации инсулина в единице суспензии препарата при следующих инъекциях. Только Инсуман Базал ГТ, по результатам исследований, имеет необходимую точность дозирования (см. рисунок)
Таким образом, можно ожидать, что потенциальные расходы на другие, кроме Инсумана, препараты инсулина НПХ, могут быть несколько выше вследствие возможного увеличения их дозировок из-за плохого перемешивания. Необходимо уделять больше внимания технике инъекций как при первичном, так и при повторном обучении больных (особенно применяющих инсулин НПХ) процедуре его эффективного перемешивания. Особенную озабоченность в связи с этим вызывают неблагоприятные клинические эффекты гипогликемий, равно как и затраты здравоохранения на их лечение. Стоимость лечения тяжелой гипогликемии, включая вызов скорой/неотложной помощи, составляет, по некоторым оценкам, 12 тыс. руб. [15].
Появление одноразовых шприц-ручек SoloSTAR намного облегчило жизнь как пациентам, так и эндокринологам. Потенциальные экономические преимущества использования данной шприц-ручки представляют интерес для рационального использования средств, выделяемых на лекарственное обеспечение.
Сегодня расскажем о главных ошибках при использовании инсулиновых шприц-ручек, которые не стоит допускать.
По неопытности или невнимательности можно перепутать шприц-ручку с инсулином (ультра)короткого действия со шприц-ручкой с инсулином длительного действия. Во избежание подобного, старайтесь держать щприц-ручки разного назначения отдельно друг от друга и/или маркировать цветом (маркером или наклейкой).
Передача своей шприц-ручки для использования другому лицу. Шприц-ручка – средство для индивидуального использования. Даже если поменять иголку, риск передачи инфекционных заболеваний сохраняется.
Нарушение правил хранения инсулина. Запасы инсулина следует держать в холодильнике при температуре 2- 6°С. Шприц-ручку, которую используете, можно хранить при комнатной температуре не больше 1 месяца, вдали от источников тепла и солнечных лучей.
Избегайте нагревания и замораживания инсулина.
Нарушение техники инъекции инсулина: не забывайте менять места инъекций, каждый раз надевать новую иглу и заполнять ее инсулином (на 2ЕД) до появления капли, удерживать иглу под кожей не менее 6 секунд после введения инсулина.
Увеличение дозы инсулина длительного действия по причине высокого сахара крови перед сном. Базальный инсулин не предназначен для снижения сахара крови, он необходим для предотвращения повышения глюкозы крови натощак. Если у вас перед сном высокий сахар, сделайте подколку небольшой дозы инсулина ультракороткого действия и пересмотрите, правильно ли вы рассчитываете дозу инсулина на ужин.
При подсчете очередной дозы инсулина (ультра)короткого действия перед едой или «на снижение» гликемии забывают учитывать время, которое прошло с предыдущей инъекции инсулина. Если прошло менее 4 часов, в крови еще есть активный инсулин. Помните об этом при расчете очередной дозы инсулина (ультра)короткого действия — это позволит избежать гипогликемии.
Информация, представленная в материале, не является медицинской консультацией и не может заменить визит к врачу.
Д.м.н., проф. Лобанова Е.Г., к.м.н. Чекалина Н.Д.
Инсулин (от лат. insula — островок) является белково-пептидным гормоном, вырабатываемым β-клетками островков Лангерганса поджелудочной железы. В физиологических условиях в β-клетках инсулин образуется из препроинсулина — одноцепочечного белка-предшественника, состоящего из 110 аминокислотных остатков. После переноса через мембрану шероховатого эндоплазматического ретикулума от препроинсулина отщепляется сигнальный пептид из 24 аминокислот и образуется проинсулин. Длинная цепь проинсулина в аппарате Гольджи упаковывается в гранулы, где в результате гидролиза отщепляются четыре основных аминокислотных остатка с образованием инсулина и С-концевого пептида (физиологическая функция С-пептида неизвестна).
Молекула инсулина состоит из двух полипептидных цепей. Одна из них содержит 21 аминокислотный остаток (цепь А), вторая — 30 аминокислотных остатков (цепь В). Цепи соединены двумя дисульфидными мостиками. Третий дисульфидный мостик сформирован внутри цепи А. Общая молекулярная масса молекулы инсулина — около 5700. Аминокислотная последовательность инсулина считается консервативной. У большинства видов имеется один ген инсулина, кодирующий один белок. Исключение составляют крысы и мыши (имеют по два гена инсулина), у них образуются два инсулина, отличающиеся двумя аминокислотными остатками В-цепи.
Первичная структура инсулина у разных биологических видов, в т.ч. и у различных млекопитающих, несколько различается. Наиболее близкий к структуре инсулина человека — свиной инсулин, который отличается от человеческого одной аминокислотой (у него в цепи В вместо остатка аминокислоты треонина содержится остаток аланина). Бычий инсулин отличается от человеческого тремя аминокислотными остатками.
Историческая справка. В 1921 г. Фредерик Г. Бантинг и Чарльз Г. Бест, работая в лаборатории Джона Дж. Р. Маклеода в Университете Торонто, выделили из поджелудочной железы экстракт (как позже выяснилось, содержащий аморфный инсулин), который снижал уровень глюкозы в крови у собак с экспериментальным сахарным диабетом. В 1922 г. экстракт поджелудочной железы ввели первому пациенту — 14-летнему Леонарду Томпсону, больному диабетом, и тем самым спасли ему жизнь. В 1923 г. Джеймс Б. Коллип разработал методику очистки экстракта, выделяемого из поджелудочной железы, что в дальнейшем позволило получать из поджелудочных желез свиней и крупного рогатого скота активные экстракты, дающие воспроизводимые результаты. В 1923 г. Бантинг и Маклеод за открытие инсулина были удостоены Нобелевской премии по физиологии и медицине. В 1926 г. Дж. Абель и В. Дю-Виньо получили инсулин в кристаллическом виде. В 1939 г. инсулин был впервые одобрен FDA (Food and Drug Administration). Фредерик Сэнгер полностью расшифровал аминокислотную последовательность инсулина (1949–1954 гг.) В 1958 г. Сэнгеру была присуждена Нобелевская премия за работы по расшифровке структуры белков, особенно инсулина. В 1963 г. был синтезирован искусственный инсулин. Первый рекомбинантный человеческий инсулин был одобрен FDA в 1982 г. Аналог инсулина ультракороткого действия (инсулин лизпро) был одобрен FDA в 1996 г.
Механизм действия. В реализации эффектов инсулина ведущую роль играет его взаимодействие со специфическими рецепторами, локализующимися на плазматической мембране клетки, и образование инсулин-рецепторного комплекса. В комплексе с инсулиновым рецептором инсулин проникает в клетку, где оказывает влияние на процессы фосфорилирования клеточных белков и запускает многочисленные внутриклеточные реакции.
У млекопитающих инсулиновые рецепторы находятся практически на всех клетках — как на классических клетках-мишенях инсулина (гепатоциты, миоциты, липоциты), так и на клетках крови, головного мозга и половых желез. Число рецепторов на разных клетках колеблется от 40 (эритроциты) до 300 тыс. (гепатоциты и липоциты). Рецептор инсулина постоянно синтезируется и распадается, время его полужизни составляет 7–12 ч.
Рецептор инсулина представляет собой крупный трансмембранный гликопротеин, состоящий из двух α-субъединиц с молекулярной массой 135 кДа (каждая содержит 719 или 731 аминокислотный остаток в зависимости от сплайсинга мРНК) и двух β-субъединиц с молекулярной массой 95 кДа (по 620 аминокислотных остатков). Субъединицы соединены между собой дисульфидными связями и образуют гетеротетрамерную структуру β-α-α-β. Альфа-субъединицы расположены внеклеточно и содержат участки, связывающие инсулин, являясь распознающей частью рецептора. Бета-субъединицы образуют трансмембранный домен, обладают тирозинкиназной активностью и выполняют функцию преобразования сигнала. Связывание инсулина с α-субъединицами инсулинового рецептора приводит к стимуляции тирозинкиназной активности β-субъединиц путем аутофосфорилирования их тирозиновых остатков, происходит агрегация α,β-гетеродимеров и быстрая интернализация гормон-рецепторных комплексов. Активированный рецептор инсулина запускает каскад биохимических реакций, в т.ч. фосфорилирование других белков внутри клетки. Первой из таких реакций является фосфорилирование четырех белков, называемых субстратами рецептора инсулина (insulin receptor substrate), — IRS-1, IRS-2, IRS-3 и IRS-4.
Фармакологические эффекты инсулина. Инсулин оказывает влияние практически на все органы и ткани. Однако его главными мишенями служат печень, мышечная и жировая ткань.
Эндогенный инсулин — важнейший регулятор углеводного обмена, экзогенный — специфическое сахаропонижающее средство. Влияние инсулина на углеводный обмен связано с тем, что он усиливает транспорт глюкозы через клеточную мембрану и ее утилизацию тканями, способствует превращению глюкозы в гликоген в печени. Инсулин, кроме того, угнетает эндогенную продукцию глюкозы за счет подавления гликогенолиза (расщепление гликогена до глюкозы) и глюконеогенеза (синтез глюкозы из неуглеводных источников — например из аминокислот, жирных кислот ). Помимо гипогликемического, инсулин оказывает ряд других эффектов.
Влияние инсулина на жировой обмен проявляется в угнетении липолиза, что приводит к снижению поступления свободных жирных кислот в кровоток. Инсулин препятствует образованию кетоновых тел в организме. Инсулин усиливает синтез жирных кислот и их последующую эстерификацию.
Инсулин участвует в метаболизме белков: увеличивает транспорт аминокислот через клеточную мембрану, стимулирует синтез пептидов, уменьшает расход тканями белка, тормозит превращение аминокислот в кетокислоты.
Действие инсулина сопровождается активацией или ингибированием ряда ферментов: стимулируются гликогенсинтетаза, пируват-дегидрогеназа, гексокиназа, ингибируются липазы (и гидролизующая липиды жировой ткани, и липопротеин-липаза, уменьшающая «помутнение» сыворотки крови после приема богатой жирами пищи).
В физиологической регуляции биосинтеза и секреции инсулина поджелудочной железой главную роль играет концентрация глюкозы в крови: при повышении ее содержания секреция инсулина усиливается, при снижении — замедляется. На секрецию инсулина, кроме глюкозы, оказывают влияние электролиты (особенно ионы Ca2+), аминокислоты (в т.ч. лейцин и аргинин), глюкагон, соматостатин.
Фармакокинетика. Препараты инсулина вводят п/к, в/м или в/в (в/в вводят только инсулины короткого действия и только при диабетической прекоме и коме). Нельзя вводить в/в суспензии инсулина. Температура вводимого инсулина должна соответствовать комнатной, т.к. холодный инсулин всасывается медленнее. Наиболее оптимальным способом для постоянной инсулинотерапии в клинической практике является п/к введение.
Полнота всасывания и начало эффекта инсулина зависят от места введения (обычно инсулин вводят в область живота, бедра, ягодицы, верхнюю часть рук), дозы (объема вводимого инсулина), концентрации инсулина в препарате и др.
Скорость всасывания инсулина в кровь из места п/к введения зависит от ряда факторов — типа инсулина, места инъекции, скорости местного кровотока, местной мышечной активности, количества вводимого инсулина (в одно место рекомендуется вводить не более 12–16 ЕД препарата). Быстрее всего инсулин поступает в кровь из подкожной клетчатки передней брюшной стенки, медленнее — из области плеча, передней поверхности бедра и еще медленнее — из подлопаточной области и ягодицы. Это связано со степенью васкуляризации подкожной жировой клетчатки перечисленных областей. Профиль действия инсулина подвержен значительным колебаниям как у различных людей, так и у одного и того же человека.
В крови инсулин связывается с альфа- и бета-глобулинами, в норме — 5–25%, но связывание может возрастать при лечении из-за появления сывороточных антител (выработка антител к экзогенному инсулину приводит к инсулинорезистентности; при использовании современных высокоочищенных препаратов инсулинорезистентность возникает редко). T1/2 из крови составляет менее 10 мин. Большая часть поступившего в кровоток инсулина подвергается протеолитическому распаду в печени и почках. Быстро выводится из организма почками (60%) и печенью (40%); менее 1,5% выводится с мочой в неизмененном виде.
Препараты инсулина, применяемые в настоящее время, отличаются по ряду признаков, в т.ч. по источнику происхождения, длительности действия, pH раствора (кислые и нейтральные), наличием консервантов (фенол, крезол, фенол-крезол, метилпарабен), концентрацией инсулина — 40, 80, 100, 200, 500 ЕД/мл.
Классификация. Инсулины обычно классифицируют по происхождению (бычий, свиной, человеческий, а также аналоги человеческого инсулина) и продолжительности действия.
В зависимости от источников получения различают инсулины животного происхождения (главным образом препараты свиного инсулина), препараты инсулина человека полусинтетические (получают из свиного инсулина методом ферментативной трансформации), препараты инсулина человека генно-инженерные (ДНК-рекомбинантные, получаемые методом генной инженерии).
Для медицинского применения инсулин ранее получали в основном из поджелудочных желез крупного рогатого скота, затем из поджелудочных желез свиней, учитывая, что свиной инсулин более близок к инсулину человека. Поскольку бычий инсулин, отличающийся от человеческого тремя аминокислотами, достаточно часто вызывает аллергические реакции, на сегодняшний день он практически не применяется. Свиной инсулин, отличающийся от человеческого одной аминокислотой, реже вызывает аллергические реакции. В лекарственных препаратах инсулина при недостаточной очистке могут присутствовать примеси (проинсулин, глюкагон, соматостатин, белки, полипептиды), способные вызывать различные побочные реакции. Современные технологии позволяют получать очищенные (монопиковые — хроматографически очищенные с выделением «пика» инсулина), высокоочищенные (монокомпонентные) и кристаллизованные препараты инсулина. Из препаратов инсулина животного происхождения предпочтение отдается монопиковому инсулину, получаемому из поджелудочной железы свиней. Получаемый методами генной инженерии инсулин полностью соответствует аминокислотному составу инсулина человека.
Активность инсулина определяют биологическим методом (по способности понижать содержание глюкозы в крови у кроликов) или физико-химическим методом (путем электрофореза на бумаге или методом хроматографии на бумаге). За одну единицу действия, или международную единицу, принимают активность 0,04082 мг кристаллического инсулина. Поджелудочная железа человека содержит до 8 мг инсулина (примерно 200 ЕД).
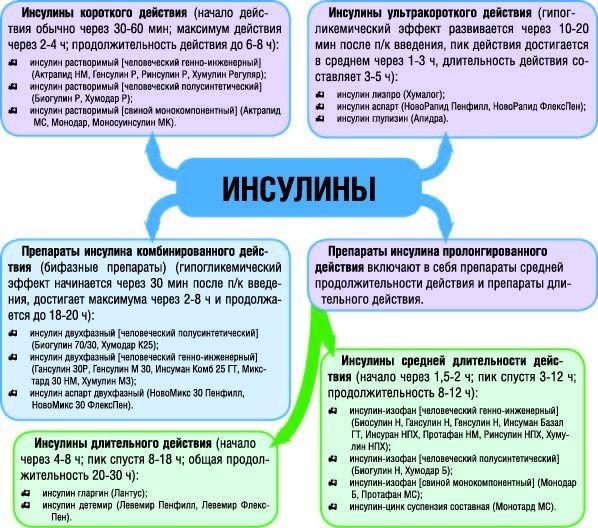
Препараты инсулина по длительности действия подразделяют на препараты короткого и ультракороткого действия — имитируют нормальную физиологическую секрецию инсулина поджелудочной железой в ответ на стимуляцию, препараты средней продолжительности и препараты длительного действия — имитируют базальную (фоновую) секрецию инсулина, а также комбинированные препараты (сочетают оба действия).
Различают следующие группы:
Инсулины ультракороткого действия (гипогликемический эффект развивается через 10–20 мин после п/к введения, пик действия достигается в среднем через 1–3 ч, длительность действия составляет 3–5 ч):
— инсулин лизпро (Хумалог);
— инсулин аспарт (НовоРапид Пенфилл, НовоРапид ФлексПен);
— инсулин глулизин (Апидра).
Инсулины короткого действия (начало действия обычно через 30–60 мин; максимум действия через 2–4 ч; продолжительность действия до 6–8 ч):
— инсулин растворимый [человеческий генно-инженерный] (Актрапид HМ, Генсулин Р, Ринсулин Р, Хумулин Регуляр);
— инсулин растворимый [человеческий полусинтетический] (Биогулин Р, Хумодар Р);
— инсулин растворимый [свиной монокомпонентный] (Актрапид МС, Монодар, Моносуинсулин МК).
Препараты инсулина пролонгированного действия — включают в себя препараты средней продолжительности действия и препараты длительного действия.
Инсулины средней длительности действия (начало через 1,5–2 ч; пик спустя 3–12 ч; продолжительность 8–12 ч):
— инсулин-изофан [человеческий генно-инженерный] (Биосулин Н, Гансулин Н, Генсулин Н, Инсуман Базал ГТ, Инсуран НПХ, Протафан НМ, Ринсулин НПХ, Хумулин НПХ);
— инсулин-изофан [человеческий полусинтетический] (Биогулин Н, Хумодар Б);
— инсулин-изофан [свиной монокомпонентный] (Монодар Б, Протафан МС);
— инсулин-цинк суспензия составная (Монотард МС).
Инсулины длительного действия (начало через 4–8 ч; пик спустя 8–18 ч; общая продолжительность 20–30 ч):
— инсулин гларгин (Лантус);
— инсулин детемир (Левемир Пенфилл, Левемир ФлексПен).
Препараты инсулина комбинированного действия (бифазные препараты) (гипогликемический эффект начинается через 30 мин после п/к введения, достигает максимума через 2–8 ч и продолжается до 18–20 ч):
— инсулин двухфазный [человеческий полусинтетический] (Биогулин 70/30, Хумодар K25);
— инсулин двухфазный [человеческий генно-инженерный] (Гансулин30Р, Генсулин М 30, Инсуман Комб 25 ГТ, Микстард 30 НМ, Хумулин М3);
— инсулин аспарт двухфазный (НовоМикс 30 Пенфилл, НовоМикс 30 ФлексПен).
Инсулины ультракороткого действия — аналоги инсулина человека. Известно, что эндогенный инсулин в β-клетках поджелудочной железы, а также молекулы гормона в выпускаемых растворах инсулина короткого действия полимеризованы и представляют собой гексамеры. При п/к введении гексамерные формы всасываются медленно и пик концентрации гормона в крови, аналогичный таковому у здорового человека после еды, создать невозможно. Первым коротко действующим аналогом инсулина, который всасывается из подкожной клетчатки в 3 раза быстрее, чем человеческий инсулин, был инсулин лизпро. Инсулин лизпро — производное человеческого инсулина, полученное путем перестановки двух аминокислотных остатков в молекуле инсулина (лизин и пролин в положениях 28 и 29 В-цепи). Модификация молекулы инсулина нарушает образование гексамеров и обеспечивает быстрое поступление препарата в кровь. Почти сразу после п/к введения в тканях молекулы инсулина лизпро в виде гексамеров быстро диссоциируют на мономеры и поступают в кровь. Другой аналог инсулина — инсулин аспарт — был создан путем замены пролина в положении В28 на отрицательно заряженную аспарагиновую кислоту. Подобно инсулину лизпро, после п/к введения он также быстро распадается на мономеры. В инсулине глулизине замещение аминокислоты аспарагин человеческого инсулина в позиции В3 на лизин и лизина в позиции В29 на глутаминовую кислоту также способствует более быстрой абсорбции. Аналоги инсулина ультракороткого действия можно вводить непосредственно перед приемом пищи или после еды.
Инсулины короткого действия (их называют также растворимыми) — это растворы в буфере с нейтральными значениями pH (6,6–8,0). Они предназначены для подкожного, реже — внутримышечного введения. При необходимости их вводят также внутривенно. Они оказывают быстрое и относительно непродолжительное гипогликемическое действие. Эффект после подкожной инъекции наступает через 15–20 мин, достигает максимума через 2 ч; общая продолжительность действия составляет примерно 6 ч. Ими пользуются в основном в стационаре в ходе установления необходимой для больного дозы инсулина, а также когда требуется быстрый (ургентный) эффект — при диабетической коме и прекоме. При в/в введении T1/2 составляет 5 мин, поэтому при диабетической кетоацидотической коме инсулин вводят в/в капельно. Препараты инсулина короткого действия применяют также в качестве анаболических средств и назначают, как правило, в малых дозах (по 4–8 ЕД 1–2 раза в день).
Инсулины средней длительности действия хуже растворимы, медленнее всасываются из подкожной клетчатки, вследствие чего обладают более длительным эффектом. Продолжительное действие этих препаратов достигается наличием специального пролонгатора — протамина (изофан, протафан, базал) или цинка. Замедление всасывания инсулина в препаратах, содержащих инсулин цинк суспензию составную, обусловлено наличием кристаллов цинка. НПХ-инсулин (нейтральный протамин Хагедорна, или изофан) представляет собой суспензию, состоящую из инсулина и протамина (протамин — белок, изолированный из молок рыб) в стехиометрическом соотношении.
К инсулинам длительного действия относится инсулин гларгин — аналог человеческого инсулина, полученный методом ДНК-рекомбинантной технологии — первый препарат инсулина, который не имеет выраженного пика действия. Инсулин гларгин получают путем двух модификаций в молекуле инсулина: заменой в позиции 21 А-цепи (аспарагин) на глицин и присоединением двух остатков аргинина к С-концу В-цепи. Препарат представляет собой прозрачный раствор с рН 4. Кислый рН стабилизирует гексамеры инсулина и обеспечивает длительное и предсказуемое всасывание препарата из подкожной клетчатки. Однако из-за кислого рН инсулин гларгин нельзя комбинировать с инсулинами короткого действия, которые имеют нейтральный рН. Однократное введение инсулина гларгина обеспечивает 24-часовой беспиковый гликемический контроль. Большинство препаратов инсулина обладают т.н. «пиком» действия, отмечающимся, когда концентрация инсулина в крови достигает максимума. Инсулин гларгин не обладает выраженным пиком, поскольку высвобождается в кровоток с относительно постоянной скоростью.
Препараты инсулина пролонгированного действия выпускаются в различных лекарственных формах, оказывающих гипогликемический эффект разной продолжительности (от 10 до 36 ч). Пролонгированный эффект позволяет уменьшить число ежедневных инъекций. Выпускаются они обычно в виде суспензий, вводимых только подкожно или внутримышечно. При диабетической коме и прекоматозных состояниях пролонгированные препараты не применяют.
Комбинированные препараты инсулина представляют собой суспензии, состоящие из нейтрального растворимого инсулина короткого действия и инсулина-изофан (средней длительности действия) в определенных соотношениях. Такое сочетание инсулинов разной продолжительности действия в одном препарате позволяет избавить пациента от двух инъекций при раздельном использовании препаратов.
Показания. Основным показанием к применению инсулина является сахарный диабет типа 1, однако в определенных условиях его назначают и при сахарном диабете типа 2, в т.ч. при резистентности к пероральным гипогликемическим средствам, при тяжелых сопутствующих заболеваниях, при подготовке к оперативным вмешательствам, диабетической коме, при диабете у беременных. Инсулины короткого действия применяют не только при сахарном диабете, но и при некоторых других патологических процессах, например, при общем истощении (в качестве анаболического средства), фурункулезе, тиреотоксикозе, при заболеваниях желудка (атония, гастроптоз), хроническом гепатите, начальных формах цирроза печени, а также при некоторых психических заболеваниях (введение больших доз инсулина — т.н. гипогликемическая кома); иногда он используется как компонент «поляризующих» растворов, используемых для лечения острой сердечной недостаточности.
Инсулин является основным специфическим средством терапии сахарного диабета. Лечение сахарного диабета проводится по специально разработанным схемам с использованием препаратов инсулина разной продолжительности действия. Выбор препарата зависит от тяжести и особенностей течения заболевания, общего состояния больного и от скорости наступления и продолжительности сахароснижающего действия препарата.
Все препараты инсулина применяются при условии обязательного соблюдения диетического режима с ограничением энергетической ценности пищи (от 1700 до 3000 ккал).
При определении дозы инсулина руководствуются уровнем гликемии натощак и в течение суток, а также уровнем глюкозурии в течение суток. Окончательный подбор дозы проводится под контролем снижения гипергликемии, глюкозурии, а также общего состояния больного.
Противопоказания. Инсулин противопоказан при заболеваниях и состояниях, протекающих с гипогликемией (например инсулинома), при острых заболеваниях печени, поджелудочной железы, почек, язве желудка и двенадцатиперстной кишки, декомпенсированных пороках сердца, при острой коронарной недостаточности и некоторых других заболеваниях.
Применение при беременности. Основным медикаментозным методом лечения сахарного диабета во время беременности является инсулинотерапия, которая проводится под тщательным контролем. При сахарном диабете типа 1 продолжают лечение инсулином. При сахарном диабете типа 2 отменяют пероральные гипогликемические средства и проводят диетотерапию.
Гестационный сахарный диабет (диабет беременных) — это нарушение углеводного обмена, впервые возникшее во время беременности. Гестационный сахарный диабет сопровождается повышенным риском перинатальной смертности, частоты врожденных уродств, а также риском прогрессирования диабета через 5–10 лет после родов. Лечение гестационного сахарного диабета начинают с диетотерапии. При неэффективности диетотерапии применяют инсулин.
Для пациенток с ранее имевшимся или гестационным сахарным диабетом важно в течение всей беременности поддерживать адекватную регуляцию метаболических процессов. Потребность в инсулине может уменьшаться в I триместре беременности и увеличиваться во II–III триместрах. Во время родов и непосредственно после них потребность в инсулине может резко снизиться (возрастает риск развития гипогликемии). В этих условиях существенное значение имеет тщательный контроль содержания глюкозы в крови.
Инсулин не проникает через плацентарный барьер. Однако материнские IgG-антитела к инсулину проходят через плаценту и, вероятно, могут вызывать гипергликемию у плода за счет нейтрализации секретируемого у него инсулина. С другой стороны, нежелательная диссоциация комплексов инсулин–антитело может привести к гиперинсулинемии и гипогликемии у плода или новорожденного. Показано, что переход с препаратов бычьего/свиного инсулина на монокомпонентные препараты сопровождается снижением титра антител. В связи с этим при беременности рекомендуют использовать только препараты инсулина человека.
Аналоги инсулина (как и другие недавно разработанные средства) с осторожностью назначают при беременности, хотя достоверных данных о неблагоприятном воздействии нет. В соответствии с общепризнанными рекомендациями FDA (Food and Drug Administration), определяющими возможность применения ЛС при беременности, препараты инсулинов по действию на плод относятся к категории B (изучение репродукции на животных не выявило неблагоприятного действия на плод, а адекватных и строго контролируемых исследований у беременных женщин не проведено), либо к категории C (изучение репродукции на животных выявило неблагоприятное действие на плод, а адекватных и строго контролируемых исследований у беременных женщин не проведено, однако потенциальная польза, связанная с применением ЛС у беременных, может оправдывать его использование, несмотря на возможный риск). Так, инсулин лизпро относится к классу B, а инсулин аспарт и инсулин гларгин — к классу C.
Осложнения инсулинотерапии. Гипогликемия. Введение слишком высоких доз, а также недостаток поступления с пищей углеводов могут вызвать нежелательное гипогликемическое состояние, может развиться гипогликемическая кома с потерей сознания, судорогами и угнетением сердечной деятельности. Гипогликемия может также развиться в связи с действием дополнительных факторов, которые увеличивают чувствительность к инсулину (например надпочечниковая недостаточность, гипопитуитаризм) или увеличивают захват глюкозы тканями (физическая нагрузка).
К ранним симптомам гипогликемии, которые в значительной степени связаны с активацией симпатической нервной системы (адренергическая симптоматика) относятся тахикардия, холодный пот, дрожь, с активацией парасимпатической системы — сильный голод, тошнота, а также ощущение покалывания в области губ и языка. При первых признаках гипогликемии необходимо проведение срочных мероприятий: больной должен выпить сладкий чай или съесть несколько кусков сахара. При гипогликемической коме в вену вводят 40% раствор глюкозы в количестве 20–40 мл и более, пока больной не выйдет из коматозного состояния (обычно не более 100 мл). Снять гипогликемию можно также внутримышечным или подкожным введением глюкагона.
Увеличение массы тела при инсулинотерапии связано с устранением глюкозурии, увеличением реальной калорийности пищи, повышением аппетита и стимуляцией липогенеза под действием инсулина. При соблюдении принципов рационального питания этого побочного эффекта можно избежать.
Применение современных высокоочищенных препаратов гормона (особенно генно-инженерных препаратов человеческого инсулина) относительно редко приводит к развитию инсулинорезистентности и явлениям аллергии, однако такие случаи не исключены. Развитие острой аллергической реакции требует проведения немедленной десенсибилизирующей терапии и замены препарата. При развитии реакции на препараты бычьего/свиного инсулина следует заменить их препаратами инсулина человека. Местные и системные реакции (зуд, локальная или системная сыпь, образование подкожных узелков в месте инъекции) связаны с недостаточной очисткой инсулина от примесей или с применением бычьего или свиного инсулина, отличающихся по аминокислотной последовательности от человеческого.
Самые частые аллергические реакции — кожные, опосредуемые IgE-антителами. Изредка наблюдаются системные аллергические реакции, а также инсулинорезистентность, опосредуемые IgG-антителами.
Нарушение зрения. Преходящие нарушения рефракции глаза возникают в самом начале инсулинотерапии и проходят самостоятельно через 2–3 недели.
Отеки. В первые недели терапии возникают также преходящие отеки ног в связи с задержкой жидкости в организме, т.н. инсулиновые отеки.
К местным реакциям относят липодистрофию в месте повторных инъекций (редкое осложнение). Выделяют липоатрофию (исчезновение отложений подкожного жира) и липогипертрофию (увеличение отложения подкожного жира). Эти два состояния имеют разную природу. Липоатрофия — иммунологическая реакция, обусловленная главным образом введением плохо очищенных препаратов инсулина животного происхождения, в настоящее время практически не встречается. Липогипертрофия развивается и при использовании высокоочищенных препаратов человеческого инсулина и может возникать при нарушении техники введения (холодный препарат, попадание спирта под кожу), а также вследствие анаболического местного действия самого препарата. Липогипертрофия создает косметический дефект, что является проблемой для пациентов. Кроме того, из-за этого дефекта нарушается всасывание препарата. Для предупреждения развития липогипертрофии рекомендуется постоянно менять места инъекций в пределах одной области, оставляя расстояние между двумя проколами не менее 1 см.
Могут отмечаться такие местные реакции, как боль в месте введения.
Взаимодействие. Препараты инсулина можно комбинировать друг с другом.
Многие ЛС могут вызывать гипо- или гипергликемию, либо изменять реакцию больного сахарным диабетом на лечение. Следует учитывать взаимодействие, возможное при одновременном применении инсулина с другими лекарственными средствами. Альфа-адреноблокаторы и бета-адреномиметики увеличивают секрецию эндогенного инсулина и усиливают действие препарата. Гипогликемическое действие инсулина усиливают пероральные гипогликемические средства, салицилаты, ингибиторы МАО (включая фуразолидон, прокарбазин, селегилин), ингибиторы АПФ, бромокриптин, октреотид, сульфаниламиды, анаболические стероиды (особенно оксандролон, метандиенон) и андрогены (повышают чувствительность тканей к инсулину и увеличивают резистентность тканей к глюкагону, что и приводит к гипогликемии, особенно в случае инсулинорезистентности; может понадобиться снижение дозы инсулина), аналоги соматостатина, гуанетидин, дизопирамид, клофибрат, кетоконазол, препараты лития, мебендазол, пентамидин, пиридоксин, пропоксифен, фенилбутазон, флуоксетин, теофиллин, фенфлурамин, препараты лития, препараты кальция, тетрациклины. Хлорохин, хинидин, хинин снижают деградацию инсулина и могут повышать концентрацию инсулина в крови и увеличивать риск гипогликемии.
Ингибиторы карбоангидразы (особенно ацетазоламид), стимулируя панкреатические β-клетки, способствуют высвобождению инсулина и повышают чувствительность рецепторов и тканей к инсулину; хотя одновременное использование этих ЛС с инсулином может повышать гипогликемическое действие, эффект может быть непредсказуемым.
Целый ряд ЛС вызывают гипергликемию у здоровых людей и усугубляют течение заболевания у больных сахарным диабетом. Гипогликемическое действие инсулина ослабляют: антиретровирусные ЛС, аспарагиназа, пероральные гормональные контрацептивы, глюкокортикоиды, диуретики (тиазидные, этакриновая кислота), гепарин, антагонисты Н2-рецепторов, сульфинпиразон, трициклические антидепрессанты, добутамин, изониазид, кальцитонин, ниацин, симпатомиметики, даназол, клонидин, БКК, диазоксид, морфин, фенитоин, соматотропин, тиреоидные гормоны, производные фенотиазина, никотин, этанол.
Глюкокортикоиды и эпинефрин оказывают на периферические ткани эффект, противоположный инсулину. Так, длительный прием системных глюкокортикоидов может вызывать гипергликемию, вплоть до сахарного диабета (стероидный диабет), который может наблюдаться примерно у 14% пациентов, принимающих системные кортикостероиды в течение нескольких недель или при длительном применении топических кортикостероидов. Некоторые ЛС ингибируют секрецию инсулина непосредственно (фенитоин, клонидин, дилтиазем) либо за счет уменьшения запасов калия (диуретики). Тиреоидные гормоны ускоряют метаболизм инсулина.
Наиболее значимо и часто влияют на действие инсулина бета-адреноблокаторы, пероральные гипогликемические средства, глюкокортикоиды, этанол, салицилаты.
Этанол ингибирует глюконеогенез в печени. Этот эффект наблюдается у всех людей. В связи с этим следует иметь в виду, что злоупотребление алкогольными напитками на фоне инсулинотерапии может привести к развитию тяжелого гипогликемического состояния. Небольшие количества алкоголя, принимаемого вместе с едой, обычно не вызывают проблем.
Бета-адреноблокаторы могут ингибировать секрецию инсулина, изменять метаболизм углеводов и увеличивать периферическую резистентность к действию инсулина, что приводит к гипергликемии. Однако они могут также ингибировать действие катехоламинов на глюконеогенез и гликогенолиз, что сопряжено с риском тяжелых гипогликемических реакций у больных сахарным диабетом. Более того, любой из бета-адреноблокаторов может маскировать адренергическую симптоматику, вызванную снижением уровня глюкозы в крови (в т.ч. тремор, сердцебиение), нарушая тем самым своевременное распознавание пациентом гипогликемии. Селективные бета1-адреноблокаторы (в т.ч. ацебутолол, атенолол, бетаксолол, бисопролол, метопролол) проявляют эти эффекты в меньшей степени.
НПВС и салицилаты в высоких дозах ингибируют синтез простагландина Е (который ингибирует секрецию эндогенного инсулина) и усиливают таким образом базальную секрецию инсулина, повышают чувствительность β-клеток поджелудочной железы к глюкозе; гипогликемический эффект при одновременном применении может потребовать корректировки дозы НПВС или салицилатов и/или инсулина, особенно при длительном совместном использовании.
В настоящее время выпускается значительное число инсулиновых препаратов, в т.ч. полученных из поджелудочных желез животных и синтезированных методами генной инженерии. Препаратами выбора для проведения инсулинотерапии являются генно-инженерные высокоочищенные человеческие инсулины, обладающие минимальной антигенностью (иммуногенной активностью), а также аналоги человеческого инсулина.
Препараты инсулина выпускаются в стеклянных флаконах, герметически укупоренных резиновыми пробками с алюминиевой обкаткой, в специальных т.н. инсулиновых шприцах или шприц-ручках. При использовании шприц-ручек препараты находятся в специальных флаконах-картриджах (пенфиллах).
Разрабатываются интраназальные формы инсулина и препараты инсулина для приема внутрь. При комбинации инсулина с детергентом и введении в виде аэрозоля на слизистую оболочку носа эффективный уровень в плазме достигается так же быстро, как и при в/в болюсном введении. Препараты инсулина для интраназального и перорального применения находятся на стадии разработки или проходят клинические испытания.
Литература
Базисная и клиническая фармакология/ Под ред. Б.Г. Катцунга; пер. с англ. под ред. Э.Э. Звартау: в 2 т.- М.-СПб.: Бином-Невский диалект, 1998.- Т. 2.- С. 181-194.
Балаболкин М.И., Клебанова Е.М., Креминская В.М. Сахарный диабет: современные аспекты диагностики и лечения/ Доктор; под ред. Г.Л. Вышковского.-2005.- М.: РЛС-2005, 2004.- 960 с. (Серия Регистр лекарственных средств России РЛС).
Балаболкин М.И., Петунина Н.А., Тельнова М.Э., Клебанова Е.М., Антонова К.В. Роль инсулиновой терапии в компенсации сахарного диабета// РМЖ.- 2007.- Т. 15.- №27 (308).- С. 2072-2077.
Виноградов В.М., Каткова Е.Б., Мухин Е.А. Фармакология с рецептурой/ Под ред. В.М. Виноградова.- 4-е изд, испр.- СПб.: СпецЛит, 2006.- С. 684-692.
Клиническая фармакология по Гудману и Гилману/ Под общ. ред. А.Г. Гилмана, ред. Дж. Хардман и Л. Лимберд. Пер. с англ.- М.: Практика, 2006.- С. 1286-1305.
Машковский М.Д. Лекарственные средства: в 2 т.- 14-е изд.- М.: Новая Волна, 2000.- Т. 2.- С. 13-17.
Михайлов И.Б. Настольная книга врача по клинической фармакологии: Руководство для врачей.- СПб.: Фолиант, 2001.- С. 562-570.
Рациональная фармакотерапия заболеваний эндокринной системы и нарушений обмена веществ: Рук. для практикующих врачей/ И.И. Дедов, Г.А. Мельниченко, Е.Н. Андреева, С.Д. Арапова и др.; под общ. ред. И.И. Дедова, Г.А. Мельниченко.- М.: Литтерра, 2006.- С. 30-39. (Рациональная фармакотерапия: Сер. руководство для практикующих врачей; Т. 12).
Регистр лекарственных средств России Пациент/ Под ред. Г.Л. Вышковского.- М.: РЛС-2006, 2005.- С. 68-72.
Сергеев П.В., Шимановский Н.Л., Петров В.И. Рецепторы физиологически активных веществ: Монография.- М.-Волгоград: Семь ветров, 1999.- С. 497-504.
Федеральное руководство по использованию лекарственных средств (формулярная система)/ Под ред. А.Г. Чучалина, Ю.Б. Белоусова, В.В. Яснецова.- Вып. VIII.- М.: ЭХО, 2007.- С. 354-363.
Харкевич Д.А. Фармакология: Учебник.- 7-е изд., перераб. и доп.- М.: Гэотар-Медицина, 2003.- С. 433-438.
USP dispensing information. V. 1.- 23th ed.- Micromedex, Inc., USA, 2003.- Р. 1546-1569.